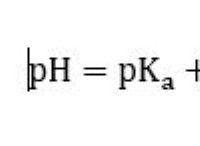1。水臭素酸(HBR)を理解してください
* HBRは強酸であり、水で完全にイオン化することを意味します。これは、すべてのHBR分子が水にプロトン(H+)を寄付することを意味します。
2。溶液の臼歯を計算します
*モラリティ(M)=溶質のモル /溶液のリットル
* m =2.48 x 10^-5モル / 0.5 l
* m =4.96 x 10^-5 m
3。水素イオン濃度([H+])を決定します
* HBRは強酸であるため、[H+]はHBR溶液の臼歯に等しくなります。
* [h+] =4.96 x 10^-5 m
4。 pH を計算します
* ph =-log [h+]
* ph =-log(4.96 x 10^-5)
*pH≈4.3
したがって、溶液のpHは約4.3です。