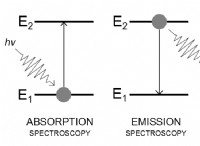
より詳細な内訳は次のとおりです。
* 滴定: 既知の濃度(滴定)の溶液が、反応が完了するまで未知の濃度(分析対象物)の溶液にゆっくりと追加されるプロセス。
* 酸ベース滴定: 酸がベースと反応する特定のタイプの滴定、またはその逆も同様です。
* インジケーター: 溶液のpHに応じて色を変える物質。
* エンドポイント: インジケータが色を変える滴定中のポイント、中和のポイントを示します。
重要な注意: エンドポイントは、等価ポイントと常に同じではありません 、これは、酸と塩基のほくろが正確に等しいポイントです。インジケーターの選択に応じて、エンドポイントと等価ポイントはわずかに異なる場合があります。
エンドポイントが重要なのはなぜですか?
エンドポイントは、分析物の未知の濃度を決定できるため、重要です。エンドポイントに到達するために使用される滴定剤の量と滴定剤の濃度を知ることにより、化学量論を使用して分析物の濃度を計算できます。
例:
既知の濃度(滴定)のNaOHの溶液で、HCl(分析物)の未知の濃度の溶液を滴定していると想像してください。 Phenolphthaleinをインジケーターとして使用します。 HCLを完全に中和するのに十分なNaOHが追加されると、フェノルフターインはピンクになり、エンドポイントを示します。次に、使用したNaOHの量とその濃度に基づいて、HClの濃度を計算できます。