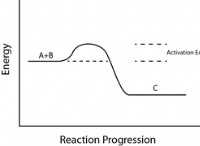
* 低エネルギー状態: 原子は、最も外側の電子シェルがいっぱいになると最も安定しています。電子を共有することにより、原子はより安定した電子構成を実現し、貴族のガスに似ています。これにより、個々の原子と比較して分子のエネルギー状態が低くなります。
* 強度の増加: 共有電子は、原子の間に強い引力を生み出し、分子で一緒に保持します。この結合は、分子の全体的な強度と安定性に貢献します。
* 新しいプロパティ: 得られる分子には、個々の原子とは異なる特性があります。これは、電子の共有が電荷の分布を変化させ、分子とその環境間の相互作用に影響を与えるためです。
例:
* 水素分子(H2): 各水素原子には1つの電子があります。これらの電子を共有することにより、どちらも完全な外殻を実現し、安定したH2分子を形成します。
* 水分子(H2O): 酸素には、外側のシェルに6つの電子があり、安定するにはさらに2つの電子が必要です。 2つの電子を2つの水素原子と共有することにより、安定した水分子を形成します。
要約すると、化学結合内の電子を共有すると、新しい特性を持つより安定した低エネルギー分子につながります。