* 極性: 水(H2O)は、電子の不均一な分布のために極性分子であり、水素側に部分的な正電荷と酸素側に部分的な負電荷を生成します。四塩化炭素(CCL4)は、炭素と塩素の電気陰性度の違いが非常に小さく、分子は対称的であるため、非極性分子です。
* "like like dislols like": 一般的な経験則は、極性物質が極性溶媒に溶解し、非極性物質が非極性溶媒に溶解することです。これは、分子間力(分子間の魅力)が同様の極性の分子間で強いためです。
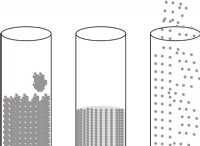
水は極性であり、四塩化炭素は非極性であるため、混和しません。 それらは2つの別々の層を形成し、密度の高いCCL4(1.59 g/ml)が底に沈殿し、上部に密度の低い水(1 g/ml)があります。