1。アニリンの共鳴効果:
*アニリン中の窒素原子の電子の孤立ペアは、ベンゼン環との共鳴に関与しています。これにより、電子密度が非局在化し、窒素原子がプロトン化に使用できなくなります。
*対照的に、アンモニアの窒素の孤独なペアは局所的であり、寄付に容易に利用できます。
2。アニリンの誘導効果:
*アニリン中のフェニル基は、誘導効果のために電子抑制です。これにより、窒素の電子密度がさらに低下し、塩基性が低下します。
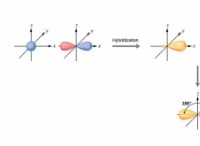
3。窒素のハイブリダイゼーション:
*アンモニアの窒素原子はSp³ハイブリダイズされていますが、アニリンではSp²ハイブリダイズします。
*SP³軌道はより拡散し、sp²軌道よりも孤立ペアをきつく保持しません。これにより、アンモニアの唯一のペアが寄付のためにより利用可能になります。
4。溶媒効果:
*アンモニアとアニリンの両方の塩基性も溶媒の影響を受けます。水溶液では、アンモニアは溶媒和が良くなっているため、より強力なベースです。
要約:
共鳴効果、誘導効果、および窒素のハイブリダイゼーションはすべて、アンモニアと比較してアニリンのより弱い塩基性に寄与します。アニリン中の窒素上の唯一のペアは、これらの要因のために寄付にはあまり利用できず、ベースが弱くなります。