これが故障です:
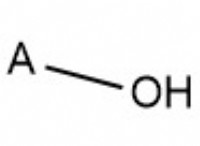
* 共有: 共有結合 、原子は原子価の電子を共有して、完全な外側のシェルを実現します。これは最も一般的なタイプの結合であり、分子の形成をもたらします。
* 獲得: イオン結合 、1つの原子が別の原子から電子を獲得します。これにより、互いに引き付ける反対に帯電したイオンが作成され、化合物が形成されます。
* 紛失: これは、1つの原子が電子を失うイオン結合でも発生します。
原子の原子が得られる傾向は、価電子電子を獲得、失い、または共有する傾向は、安定したオクテットを達成したいという欲求によって駆動されます。つまり、最も外側のシェルに8つの電子があります(水素とヘリウムを除き、2つだけが必要です)。この安定性は、化合物を個々の原子よりもエネルギー的に有利にするものです。