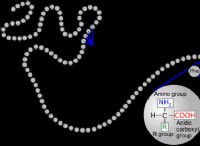
* 電気陰性の差: 極性結合結合は、関与する原子間で電気陰性度に有意な差がある場合に形成されます。 ラウリン酸(C12H24O2)には、一端にカルボニル基(C =O)を備えた炭素鎖があります。酸素原子は炭素よりもはるかに電気陰性であり、C =Oグループで強い極性共有結合をもたらします。水(H2O)では、酸素と水素の間の電気陰性度の違いも重要ですが、結合強度は他の要因に影響されます。
* 水素結合: 水は、極性の高い性質のために強い水素結合を形成します。これらの水素結合は、水の全体的な凝集強度に大きく貢献しています。ラウリン酸は、極カルボニル基を持っているが、水のように広範な水素結合ネットワークを形成していない。
* 分子サイズとファンデルワールス力: ラウリン酸は水よりも大きな分子です。その長い炭素鎖は、より強力なロンドン分散勢力(ヴァンデルワールス力の一種)に寄与し、全体的なまとまりの強さにも寄与します。
要約:
*水とラウリン酸の両方に極性の共有結合がありますが、ラウリン酸のC =O結合が強く、その大きさが大きいほど全体的な結合強度が高くなります。
*水の強力な水素結合ネットワークは優れた溶媒になりますが、それは必ずしも個々の極性結合がラウリン酸よりも強いという意味ではありません。