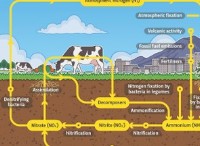
* NH4+は、アンモニア(NH3)の共役酸です: アンモニアは弱い塩基であり、プロトン(H+)を受け入れると、アンモニウムイオン(NH4+)を形成します。
* 弱い塩基の共役酸は酸性です: これは、酸塩基化学の一般的な原則です。弱い塩基が陽子を獲得すると、それは弱酸になります。
* nh4+は陽子を寄付できます: 溶液中、NH4+はプロトン(H+)を水に寄付し、酸性特性の原因となるハイドロニウムイオン(H3O+)を形成できます。
反応:
NH4 +(AQ) + H2O(L)⇌H3O +(AQ) + NH3(AQ)
結論:
溶液中のNH4+からのハイドロニウムイオン(H3O+)の形成により、酸性になります。