これが反応のバランスの取れた化学式です:
mgo(s) + 2 hcl(aq)→mgcl 2 (aq) + h 2 o(l)
ここに何が起こるかの内訳があります:
* 酸化マグネシウム(MGO) 白い固体、塩基性酸化物です。
* 塩酸(HCl) 強酸です。
*酸はベースと反応します。これは中和と呼ばれるプロセス 。
* 塩化マグネシウム(Mgcl 2 ) 水に溶ける可溶性塩です。
* 水(H 2 o) 副産物として生成されます。
観測:
*塩酸に溶解する酸化マグネシウムが観察されます。
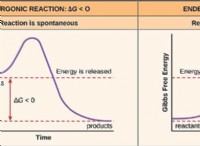
*反応が発熱すると溶液が熱くなる可能性があります(熱を放出)。
* Litmusの紙を使用すると、反応が進行するにつれて赤(酸性)から青(塩基性)に変化する溶液が変化し、酸の中和を示していることに気付くでしょう。
全体として、酸化マグネシウムと塩酸の反応は、塩化マグネシウムと水を生成する単純な酸塩基中和反応です。