bohrモデルの基本:
* 電子シェル: BOHRモデルは、シェルと呼ばれる特定のエネルギーレベルで核を周回する電子を説明しています。
* 電子構成: 各シェルは、限られた数の電子(2n²、nはシェル数)を保持できます。
* 量子ジャンプ: 電子は、エネルギー(光子)を吸収または放出することにより、貝殻の間をジャンプできます。
bohrモデルを周期表に関連付ける:
* 期間: 周期表の行(期間)は、最も高い占有電子シェルの主要な量子数(n)に対応しています。たとえば、最初の行の要素(li、be、bなど)は、n =2シェルに最も高い電子を持っています。
* グループ: カラム(グループ)は、価電子の数(最も外側のシェルの電子)の数によって決定されます。同じグループの元素は、同じ数の価電子を持っているため、同様の化学的特性を持っています。
* イオン化エネルギー: BOHRモデルは、グループの期間(増加)および下(減少)にわたるイオン化エネルギーの傾向を説明できます。 BOHRモデルのエネルギーレベルが高いということは、電子が核から遠く、除去しやすいことを意味します。
* 原子半径: BOHRモデルは、グループの期間(減少)および下(増加)にわたる原子半径の傾向を説明することもできます。期間にわたる核電荷の増加は電子をより近くに引きますが、グループに新しい電子殻を添加すると、原子半径が増加します。
制限:
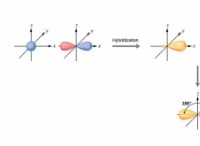
* 軌道対軌道: BOHRモデルは、円形の経路で核を周回する電子を示しています。これは単純化しすぎです。現代の量子力学は、軌道を使用した電子の挙動を表します。軌道は、電子が見つかる可能性が高い空間の3次元領域です。
* 量子力学: BOHRモデルは、d-ブロック要素とfブロック要素の存在や軌道の充填など、周期表で観察される多くの現象を説明する際に制限されています。最新の量子力学は、より正確で包括的な説明を提供します。
結論:
BOHRモデルには制限がありますが、特に電子構成、イオン化エネルギー、原子半径の観点から、周期表の基本的な傾向の一部を視覚化するのに役立つ単純化された画像を提供します。ただし、周期表をより深く理解するには、現代の量子力学の原則に依存することが重要です。