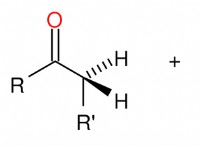
これが故障です:
* 滴定: 追加される既知の濃度のソリューション。
* 分析物: 私たちが決定したい未知の濃度のソリューション。
* 等価ポイント: 滴定剤のモルが添加されている滴定の点は、存在する分析物のモルに化学的に等しい。
* インジケーター: 同等のポイントで色を変える物質で、反応が完全であることを示しています。
それがどのように機能するか:
1.分析物の既知の体積をフラスコに入れます。
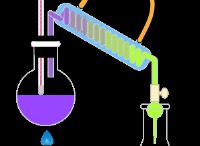
2。滴定は、底部に停止コックが付いた長い段階的なチューブであるブレットからゆっくりと追加されます。
3.インジケータは分析物溶液に追加され、滴定は色が色が変わるまで継続し、等価点を示します。
4.追加された滴定剤の量が記録されています。
5.抑制性の既知の濃度と添加容積を使用して、分析物の濃度を計算できます。
例:
塩酸(HCL)の未知の溶液の濃度を決定したいとしましょう。水酸化ナトリウム(NAOH)の標準化された溶液を滴定剤として使用できます。
NAOHソリューションをHCLソリューションにドロップすることにより、反応が完了するポイントを決定することができます。この点は、インジケータによるソリューションの色の変化によってマークされています。 NaOHの量とその既知の濃度により、HCl溶液の濃度を計算できます。
滴定は、分析化学の基本的な手法であり、酸、塩基、その他の反応性化合物を含むさまざまな物質の濃度を決定するために使用されます。