その理由は次のとおりです。
* pHは、水素イオン濃度の尺度です。 この濃度は、その温度ではなく、物質の化学組成によって決定されます。
* 温度の変化は、化学反応の速度に影響を与える可能性があります。 しかし、ほとんどの純粋な物質の場合、水素イオンの形成と解離の平衡は比較的安定しています。
例外:
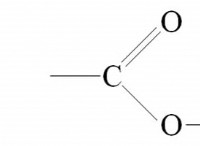
* 一部の反応は温度に敏感です。 特定の場合、加熱または冷却は反応の平衡をシフトし、pHの変化につながる可能性があります。たとえば、炭酸(H2CO3)の溶液を加熱すると、二酸化炭素(CO2)と水(H2O)に分解し、pHの減少をもたらす可能性があります。
* 弱酸または塩基を含む溶液。 弱酸と塩基のイオン化は温度依存性です。加熱はイオン化を増加させる可能性があり、弱酸のpHの減少または弱い塩基のpHの増加につながります。
結論:
ほとんどの場合、物質の加熱または冷却はそのpHに大きな影響を与えません。ただし、温度変化がpHに顕著な影響を与える可能性があるかどうかを判断するために、特定の物質とその特性を考慮することが重要です。