主な違い - イオン結合、共有結合、金属結合
債券は大きく 2 つのカテゴリに分けられます。一次結合と二次結合。一次結合は分子内の原子を保持する化学結合であり、二次結合は分子を一緒に保持する力です。一次結合には、イオン結合、共有結合、金属結合の 3 種類があります。二次結合には、分散結合、双極子結合、および水素結合が含まれます。一次結合は結合エネルギーが比較的高く、二次結合よりも安定しています。イオン共有結合と金属結合の主な違いは、それらの形成です。 イオン結合は、1 つの原子が別の原子に電子を提供するときに形成されます。共有結合は、2 つの原子がその価電子を共有するときに形成され、金属結合は、可変数の原子が金属格子内の可変数の電子を共有するときに形成されます。
この記事では、
について調べます。
1. イオン結合とは?
– 定義、形成、プロパティ
2. 共有結合とは
– 定義、形成、プロパティ
3. 金属結合とは?
– 定義、形成、プロパティ
4. イオン共有結合と金属結合の違いは何ですか? 
イオン結合とは
特定の原子は、最も外側の軌道を完全に占有することでより安定するために、電子を供与または受け取る傾向があります。最も外側の殻にほとんど電子がない原子は、電子を供与して正に帯電したイオンになる傾向がありますが、最も外側の軌道に多くの電子を持つ原子は、電子を受け取って正に帯電したイオンになる傾向があります。これらのイオンが一緒になると、イオンの反対の電荷のために引力が発生します。これらの力はイオン結合と呼ばれます。これらの安定した結合は、静電結合とも呼ばれます .イオン結合で結合した固体は結晶構造を持ち、電気伝導度が低くなります。これは、自由に移動する電子がないためです。結合は通常、電気陰性度に大きな違いがある金属と非金属の間で発生します。イオン結合材料の例には、LiF、NaCl、BeO、CaF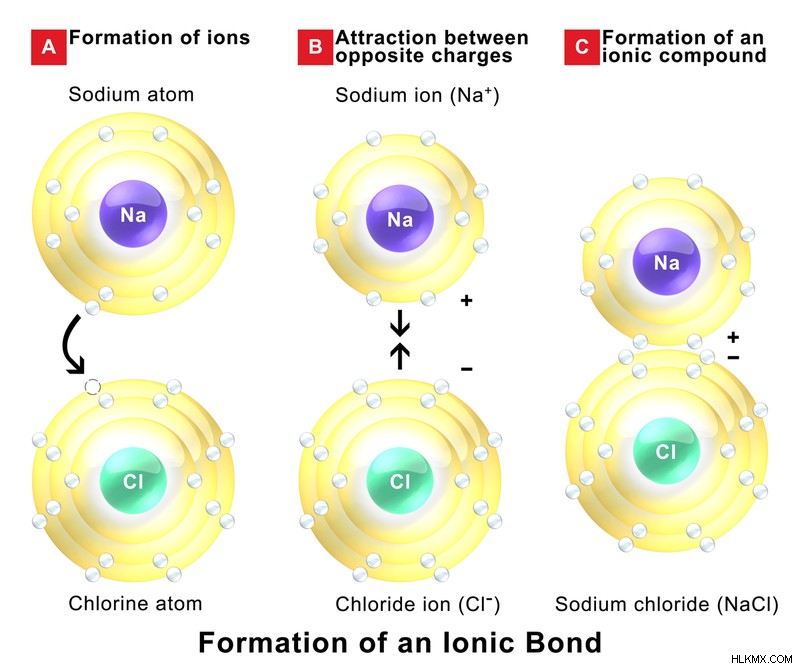
共有結合とは
共有結合は、2 つの原子が価電子を共有するときに形成されます。 2 つの原子の電気陰性度はわずかに異なります。共有結合は、同じ原子間または異なる種類の原子間で発生します。たとえば、フッ素はその外殻を完成させるために 1 つの電子を必要とするため、1 つの電子は共有結合を形成することによって別のフッ素原子と共有され、結果として F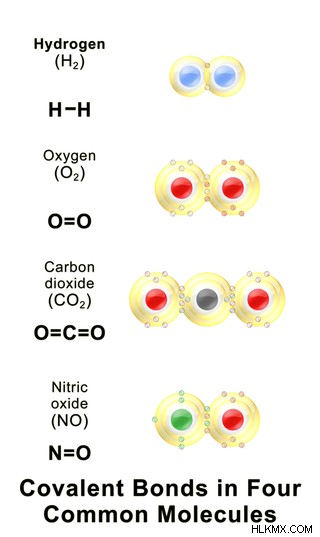
金属結合とは
金属格子では、価電子は金属原子の原子核によって緩く結合されています。したがって、価電子は原子核から放出するのに非常に低いエネルギーを必要とします。これらの電子が離れると、金属原子は正に帯電したイオンになります。これらの正に帯電したイオンは、電子雲と呼ばれる多数の負に帯電した自由に移動する電子に囲まれています。電子雲とイオンの間の引力により、静電力が形成されます。これらの力は金属結合と呼ばれます。金属結合では、金属格子内のほぼすべての原子が電子を共有します。したがって、どの原子がどの電子を共有しているかを決定する方法はありません。このため、金属結合中の電子は非局在化電子と呼ばれます。電子が自由に移動するため、金属は優れた電気伝導体として知られています。金属結合を持つ金属の例には、鉄、銅、金、銀、ニッケルなどがあります。 
イオン共有結合と金属結合の違い
定義
イオン結合: イオン結合は、負イオンと正イオンの間で発生する静電力です。
共有結合: 共有結合は、中性ガスの電子構成を得るために 2 つの元素が価電子を共有するときに生じる結合です。
金属結合: 金属結合は、負に帯電した自由に移動する電子と正に帯電した金属イオンの間の力です。
絆エネルギー
イオン結合: 結合エネルギーは金属結合よりも高いです。
共有結合: 結合エネルギーは金属結合よりも高いです。
金属結合: 結合エネルギーは他の主要な結合よりも低くなっています。
フォーメーション
イオン結合: イオン結合は、ある原子が別の原子に電子を提供するときに形成されます。
共有結合: 共有結合は、2 つの原子がその価電子を共有するときに形成されます。
金属結合: 金属結合は、可変数の原子が金属格子内で可変数の電子を共有するときに形成されます。
導電率
イオン結合: イオン結合は導電率が低いです。
共有結合: 共有結合の伝導率は非常に低いです。
金属結合: 金属結合は、非常に高い電気伝導性と熱伝導性を備えています。
融点と沸点
イオン結合: イオン結合は、融点と沸点が高くなります。
共有結合: 共有結合は融点と沸点が低くなります。
金属結合: 金属結合は融点と沸点が高いです。
物理的状態
イオン結合: イオン結合は固体状態でのみ存在します。
共有結合: 共有結合は、固体、液体、気体の形で存在します。
金属結合: 金属結合は固体の形でのみ存在します。
絆の性質
イオン結合: 結合は方向性がありません。
共有結合: 結合には方向性があります。
金属結合: 結合は方向性がありません。
硬度
イオン結合: 結晶構造のため、イオン結合は固いです。
共有結合: ダイヤモンド、シリコン、炭素を除いて、共有結合はそれほど硬くありません。
金属結合: 金属結合はそれほど固くありません。
可鍛性
イオン結合: イオン結合を持つ材料は順応性がありません.
共有結合: 共有結合を持つ材料は可鍛性がありません.
金属結合: 金属結合を持つ材料は可鍛性があります.
延性
イオン結合: イオン結合を持つ材料は延性がありません。
共有結合: 共有結合を持つ材料は延性がありません。
金属結合: 金属結合を持つ材料は延性があります。
例
イオン結合: 例には LiF、NaCl、BeO、CaF2 などがあります など
共有結合: 例には、水素ガス、窒素ガス、水分子、ダイヤモンド、シリカなどがあります。
金属結合: 例には、鉄、金、ニッケル、銅、銀、鉛などが含まれます。
参照:
クラコリス、マーク。 数学の復習を含む入門化学の基礎 .第2版N.p.:Cengage Learning、2009 年。Print.Duke、Catherine Venessa。 A.、およびクレイグ・デンバー・ウィリアムズ。 環境および地球科学のための化学 . N.p.:CRC Press, 2007. Print.Garg, S. K. 包括的なワークショップ テクノロジー . N.p.:Laxmi Publications、2009 年。印刷。 画像提供: 「Ionic Bonds」 BruceBlaus 著 – Commons Wikimedia 経由の自身の作品 (CC BY-SA 4.0) 「共有結合」 BruceBlaus 著 – Commons Wikimedia による自身の作品 (CC BY-SA 4.0) Muskid による「金属結合」 – Commons Wikimedia による自身の作品 (CC BY-SA 3.0)