これが故障です:
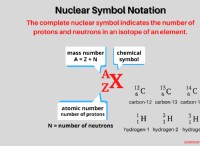
* 要素: プロトンの数で定義されています その核内。これは原子番号と呼ばれます 。
* 同位体: 同じ要素の原子(同じ原子番号)ですが、異なる数の中性子 。この違いは、原子質量に影響します 同位体の。
例:
* 炭素-12: 6個の陽子と6個の中性子
* 炭素-14: 6個の陽子と8個の中性子
どちらも6つのプロトンを持っているため、どちらも炭素原子ですが、中性子の数は異なります。これにより、炭素-14はより重く放射性になります。
キーテイクアウト:
*同じ元素の同位体は、同じ数の電子を持っているため、同じ化学的特性を持っているため、他の原子との相互作用を決定します。
*同位体は、中性子の数が異なるため、質量や放射能などの異なる物理的特性を持つことができます。
*中性子数のこの違いは、医学、考古学、原子力エネルギーなどの分野で異なる用途を持つ同位体につながります。