* 粒子サイズ: 固体粒子は通常、液体分子よりもはるかに大きいです。固体が溶けると、その粒子は肉眼では見えないイオンや分子のような小さなユニットに分解します。
* 均一な分布: 溶解した粒子は液体全体に均等に分布し、均質な混合物を作成します。これは、溶解した固体がもはや1つの領域に集中していないため、消滅するように見えることを意味します。
* 溶媒との相互作用: 溶解した固体粒子は、水素結合、双極子双極子相互作用、またはイオン双極子相互作用などの力を介して溶媒分子と相互作用します。これらの力は、溶解した粒子が再び凝集するのを防ぎ、それらを分散させます。
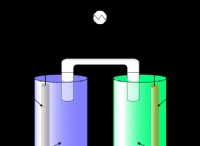
例: 水に塩(NaCl)を加えると、塩結晶壊れのイオン結合、ナトリウム(Na+)と塩化物(Cl-)イオンは水分子に囲まれます。塩はもはや固体として存在しませんが、そのイオンは水に溶けてしまい、消滅したように見えます。
注: 固体は消えているように見えますが、溶液内に存在します。これが、蒸発などのプロセスによって溶解した固体を回復できる理由です。溶解した粒子は、溶媒が蒸発するにつれて再凝集して固化します。