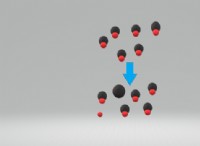
* 頻度の増加: より高い温度は、分子がより速度論的エネルギーを持っていることを意味し、より速く動き、より頻繁に衝突します。
* エネルギーの増加: また、より高い運動エネルギーは、各衝突がその背後により多くの力を持っていることを意味し、分子間のより大きなエネルギー移動につながります。
* 反応の可能性の増加: よりエネルギー的な衝突により、化学反応が発生するために必要な活性化エネルギー障壁を分子が克服する可能性が高くなります。
このように考えてみてください:じっと立っている人々のグループを想像してください(低温)。彼らはあまり衝突していません。今、それらがすべて乱暴に走り回ることを想像してください(高温)。彼らはより頻繁に衝突し、各衝突はより多くの影響を与えます。
ここに覚えておくべき重要なポイントがいくつかあります:
* 衝突理論: この理論は、温度が分子間の衝突に焦点を当てることにより反応速度にどのように影響するかを説明しています。
* 活性化エネルギー: 反応が発生するのに必要な最小エネルギー。より高い温度は、この障壁を克服するのに十分なエネルギーを持つ分子の数を増やします。
したがって、温度の上昇は、分子衝突の頻度、エネルギー、および有効性に影響を与えることにより、化学反応を加速する強力な方法です。