1。要素を特定します:
* 31個の電子を持つ原子はガリウム(GA)です 。
2。電子構成:
* 1S²2S²2P⁶3S²3p⁶4S²3d¹⁰4p¹
説明:
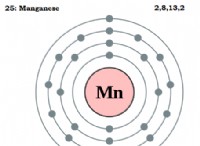
* 軌道: 電子は、軌道と呼ばれる特定のエネルギーレベルとサブレベルを占有します。
* s軌道: 最大2つの電子を保持します。
* p軌道: 最大6つの電子を保持します。
* d軌道: 最大10個の電子を保持します。
* 充填順序: 電子は、エネルギーレベルの増加に基づいて特定の順序で軌道を満たします。これは、多くの場合、Aufbau原則と対角線ルール(「矢印」ルールとも呼ばれます)で表されます。
* sublevels:
* 1s、2s、2p、3s、3p、4s、3d、4p: これらは、各エネルギーレベル内の異なるサブレベルを表します。
* SuperScripts: 上付き文字(例:1S²の²)は、各サブレベルの電子の数を示しています。
段階的に分解しましょう:
1。1S²: 最初のエネルギーレベル(n =1)には、1つのサブルベル、「S」軌道しかありません。 2つの電子を保持します。
2。2S²: 2番目のエネルギーレベル(n =2)には、2つの電子を保持する「S」軌道があります。
3。2p⁶: 2番目のエネルギーレベルには、3つの「P」軌道もあり、合計6つの電子を保持できます。
4。3S²: 3番目のエネルギーレベル(n =3)には、2つの電子を保持する「S」軌道があります。
5。3p⁶: 3番目のエネルギーレベルには、6つの電子を保持する3つの 'p'軌道もあります。
6。4S²: 4番目のエネルギーレベル(n =4)には、2つの電子を保持する「S」軌道があります。
7。3d¹⁰: 4番目のエネルギーレベルが埋め始めていますが、3Dサブレベルのエネルギーは低く、次に満たされます。 5つの「d」軌道があり、10個の電子を保持します。
8。4p¹: 4番目のエネルギーレベルには、3つの「P」軌道があります。ガリウムは、このサブレベルに1つの電子しかありません。
この構成が周期表にどのように関係しているかを確認したい場合、または他の質問がある場合はお知らせください!