水素分子

二水素としても知られる水素分子は、化学式H2の共有結合によって結合された2つの水素原子で構成される二原子分子です。水素分子は油脂の水素添加に使われ、風船の充填にも使われることがあります。水素分子は、金属表面だけでなく、炭素、ゼオライト、アルミナ、およびシリカ表面にも吸着できます。
宇宙に存在する最も豊富な原子または元素の 1 つは水素です。それは、宇宙の全原子の約 90% を占めています。原子番号は 1 で、原子量は 1.008 で、周期表のすべての元素の中で最も軽く、最小です。水素分子は一般に気体の状態で見られます。ほとんどの場合、可燃性の高い無色無臭のガスとして存在します。
水素の原子番号は 1 であるため、周期表の最初の元素です。ハロゲンやアルカリ金属と同じいくつかの特徴があります。しかし、最近のいくつかの研究では、科学者は水素が金属の形でも存在することを発見しました.他のアルカリと同様に、その最外殻には 1 つの電子が含まれており、そのイオン化エネルギーはハロゲン原子のイオン化エネルギーに似ています。
水素は自然界に大量に存在しますが、遊離状態で自然界に存在することはめったにありません。ほとんどの場合、化学化合物中の他の元素と結合しています。たとえば、水 (H2O) 分子では、H2 分子が酸素原子に結合しています。水素を燃やすと、空気中の酸素と反応して水になるのは興味深いことです。実際、この現象は水素分子にその名前を与えました。名前はギリシャ語の「ハイドロ ジーン」に由来し、水の創造者を意味します。
水素分子の発生
前述のように、H2 分子は宇宙で最も豊富に存在する元素であり、宇宙全体の質量の 70% を占めています。その分子形態では、二水素として見出されます。水素は太陽系の主要な要素でもあり、最大の惑星である土星と木星は主に水素で構成されています。結合した状態では、水素は地球と海洋の地殻の 15.3% を形成します。
水素分子の発見
ヘンリー・キャベンディッシュという英国の科学者は、1765 年に初めて水素分子を発見し、それを「可燃性空気」と名付けました。フランスの科学者アントワーヌ ラヴォアジエは、1783 年に「水素」という名前を作り出しました。
水素の同位体
水素には主に 3 つの同位体があり、それらはすべて同じ電子配置を持っています。したがって、それらの化学的性質も同じです。ただし、質量数が異なるため、水素の同位体の物理的性質はまったく異なります。以下は、水素の 3 つの同位体です:
| 同位体 | 原子量 | 原子番号 | 陽子数 | 中性子の数 |
| 重水素 | 2 | 1 | 1 | 1 |
| プロチウム | 1 | 1 | 1 | 0 |
| トリチウム | 3 | 1 | 1 | 2 |
上の表の水素分子の 3 つの同位体のうち、プロチウムは最も一般的なものであり、自然界に豊富に存在します。
周期表における水素の位置
水素はアルカリやハロゲンと同じです。それが周期表の一番上にある理由です。
水素とアルカリの類似点は何ですか?
<オール>説明:
H (Z=1) – K1
Li (Z=3) – K2、L1
ナ (Z=11) – K2、L8、M1
K (Z=19) – K2、L8、M8、N1
- グループ I A と H2 分子の両方の要素は、同じ外形 ns1 を持っています
説明:
H (Z=1) – 1s1
リー (Z=3) – 1s2、2s1
ナ (Z=11) – 1s2、2s2、2p6、3s1
K (Z=19) – 1s2、2s2、2p6、3s2、3p6、4s1
- アルカリ金属と同様に、水素もハロゲン化物を生成します。
説明:
I-A:NaCl、KBr.
水素:HCl、HI.
- 電気分解中、陰極で水素ガスが放出されます。
- 水素とアルカリ金属の酸化状態はどちらも +1 です。
- アルカリ金属のハロゲン化物と同様に、ハロゲン化水素は水性媒体中でイオン化されます。
説明:
HCl(aq)→ H+(aq) + Cl–(aq)
NaCl(aq)→ Na+(aq) + Cl–(aq)
- アルカリ金属などの非金属化合物も、水素によって形成される場合があります。
説明:
水素:H2 S
I-A:Na2 S
水素はどのようにハロゲンに似ていますか?
<オール>説明:
ハロゲン:HCl (H は非金属)
水素:H2S (S は非金属)
したがって、水素の類似性は、アルカリ金属よりもハロゲンの方が高くなります。そのため、周期表におけるその位置は正当化されません。
水素とハロゲンおよびアルカリ金属の違い:
<オール>水素の性質
水素の物理的性質
- 水素は無色、無臭、中性ガスです
- 水素は水に溶けにくい
- 引火性が高く、青い炎で燃える
- 沸点が非常に低い
水素の化学的性質
- H-H 結合は比較的強い結合エンタルピーを持っているため、室温では二水素はかなり不活性です。
- 水素原子の軌道は 1 つの電子で完結していないため、水素原子を生成するには高電気アークが必要です。
- 水素は、ほぼすべての元素と結合できます。
さまざまな形態の水素
原子状水素:
原子状水素は、電気アークに水素分子を通すと生成されます。この電気アークの周りには 2 つのタングステン電極があり、その温度は 2273K です。この過程で発生した熱は原子に蓄えられます。
H2→ 2H- 熱
反応で放出された水素原子は再び結合して H を形成します。このプロセスで大量のエネルギーが放出され、溶接目的で使用されます。
新生水素:
水素が生成されたとき、または解放されたばかりのときは、発生期水素と呼ばれます。通常の水素よりも強力な還元剤であり、はるかに反応性が高いです。
水素分子の調製方法
<オール>
2. 強い電気陽性金属との作用の反応
2Na+ + H2 SO4 —→ナ2 SO4 + H2 (水素分子2個)
2K+2HCl→ 2KCl+ H2 (水素分子2個)
3. 水と強い電気陽性金属との反応:
2Na + 2H2 O —→ 2NaOH + H2 (水素分子2個)
4. アルカリと Zn や Al などの金属との反応
6NaOH (ホット &濃縮) + 2Al —→ 2 Na3 アロ3 + 3H2
Zn + 2NaOH —→ Na2 + ZnO2 + H2 (水素分子2個)
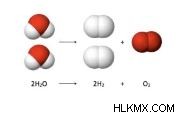
5. 水素と酸素の反応
水素が二酸素と反応すると、水が生成されます。
H2 + 12O2 →[△] 200 ∘ CH2 O発生期の水素
6. 水素と金属の反応
水素は高温で多くの金属と反応し、対応する水素化物を生成します。たとえば、
2Na + H2 (水素分子2個) →[Δ] 350 ∘ C2 NaH (水素化ナトリウム)
7.水素とハロゲンの反応
水素はハロゲンと反応してハロゲン化水素を形成します。
H2 + F2 →ダーク2HF
H2 + Cl2 → 日光 2HCl
H2 +ブラ2 → 350 ∘ C2HBr
H2 + 私2 → 2HI
8. 水素と有機化合物の反応:
水素は、特定の触媒の存在下で多くの有機化合物と反応して、商業的に重要な製品を生成します。たとえば、
- ニッケル触媒の存在下で、植物油が水素化されます。
- オレフィンのヒドロホルミル化が起こると、アルデヒドが形成され、アルコールが生成されます.
水素の使用
以下は、水素の用途の一部です:
- アンモニアの調製に使用されます。
- 水性ガスなどの燃料ガスの調製に使用されます。
- 水素は冶金で還元剤として使用されます。
- 水素の核融合反応では、大量のエネルギーが星に放出されます。
結論
水素は周期表で最も重要な元素の 1 つであり、その反応は自然界でも商業利用でも非常に重要です。したがって、それについての知識を持つことは重要です。このブログが、このトピックに関する必要な知識を得るのに役立つことを願っています.
よくある質問
Q) 発生期の水素が通常の水素よりも反応性が高いのはなぜですか?
A) 発生期の水素ガス分子は、原子状態にあるため、通常の水素よりも反応性が高く、原子は分子よりも反応性が高い.また、内圧が高くなります。
Q) 水素の同素体は何ですか?
A) 以下は、水素分子が発生する 2 つの異性体です。
<オール>Q) 水素ガス分子は空気中で燃焼しますか?
A) はい、水素ガス分子が空気中の酸素と反応して、H2O または水を生成します。その過程で、ある程度のエネルギーも放出されます。