物理的特性:
* 低沸点: 分子間力が弱い液体は、分子間の魅力を克服するためのエネルギーが少ないため、沸点が低くなります。
* 高蒸気圧: 分子間力が弱いことにより、分子は液相をより簡単に逃げることができ、蒸気圧が高くなります。
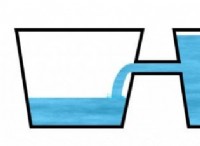
* 低粘度: 分子間力が弱い液体は、耐性が最小限に抑えられて容易に流れ、粘度が低いことを示します。
* 高揮発性: 分子間力が弱い液体は容易に蒸発し、揮発性になります。
* 低表面張力: 分子間の凝集力は弱く、表面張力が低くなります。
分子構造:
* 非極性分子: 非極性分子は、主要な分子間力としてロンドン分散力が弱い。
* 小分子: より小さな分子は相互作用の表面積が少なく、分子間力が弱くなります。
* 水素結合の欠如: 水素結合は強い分子間力であるため、それらの不在は弱い力を示しています。
例:
* エーテル: ジエチルエーテルは、沸点が低い(-34.6°C)、蒸気圧が高く、双極子双極子の相互作用とロンドン分散力が弱いため、非常に揮発性があります。
* メタン(CH4): メタンは、ロンドンの分散力が弱いだけであるため、室温でのガスです。
重要な注意:
分子間力の強度は、特定の分子と環境によって異なる可能性があることを考慮することが重要です。たとえば、ロンドンの分散力は一般的に弱いものの、多くの電子を持つ大きな分子で重要になる可能性があります。