コア コンセプト
このチュートリアルでは、イオン双極子力とイオン誘起双極子力について学習します。
他の記事で取り上げるトピック
- 陽イオンと陰イオン
- 多原子イオン
- 双極子モーメントとは
- 結合順序と結合長
- ファンデルワールス軍
語彙
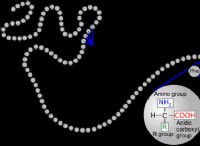
イオン – 1 つまたは複数の電子の損失または獲得により、正または負の電荷を持つ原子または分子。
ダイポール – 距離を隔てて、反対の電荷を持つ 2 つの極を持つ分子。
静電相互作用 – 荷電分子間の引力または反発相互作用。
分子間力 – 分子間の物理的な力.
イオン双極子力
イオン双極子力は静電相互作用です 完全に荷電したイオンと双極子を持つ中性分子の間。さらに、分子間力
イオンの電荷は、分子のどの部分が引き付けられ、反発するかを決定します。したがって、陽イオンは分子の部分的に負の端を引き付けますが、陰イオンは分子の部分的に正の端を引き付けます。
イオン双極子力の例:
Na (ナトリウムイオン) と H2 O(水分子)
Na:陽イオン
H2 の部分的に肯定的な終わり O:H 原子から
H2 の部分的に負の終了 O:O原子から
→ ナトリウムは水分子の酸素原子を引き付け、水素原子をはじきます。

イオン誘起双極子力
イオン誘起双極子力は、イオンが非極性分子と相互作用するときに生じる弱い引力です。さらに、完全に荷電したイオンが非極性分子に近づくと、電子が反応し、分子は双極子を形成します。したがって、イオンは非極性分子を分極します。
陽イオンは電子雲を引き寄せることによって分子を分極させますが、陰イオンは電子雲を反発させることによって分極させます。
イオン誘起双極子力の例:
いいえ3 (硝酸イオン) と I2 (ヨウ素分子)
NO3 :陰イオン
私2 :非極性分子
→ 硝酸イオンが存在すると、ヨウ素分子が分極します。