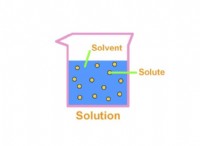
ただし、不純物 水の中では、導電性にするものです。これらの不純物は、多くの場合、溶解した塩、酸、または塩基です。これらの物質が水に溶解すると、イオンに分離します。たとえば、テーブル塩(NaCl)は、ナトリウムイオン(Na+)および塩化物イオン(Cl-)に溶解します。
これがどのように機能しますか:
1。溶解イオン: 塩、酸、塩基などの不純物は、水に溶解すると、正の帯電イオン(陽イオン)および負に帯電したイオン(アニオン)に解離します。
2。電流: 電圧が水面に加えられると、これらのイオンは動き始めます。 カチオンは負の電極(カソード)に向かって移動し、陰イオンは正の電極(アノード)に向かって移動します。荷電粒子のこの動きは、電流を構成します。
3。導電率: 水中に存在するイオンが多いほど、導電率が高くなります。これが、溶解した鉱物を含む水道水が純水よりも優れた電気導体である理由です。
重要な注意: 少量の不純物でさえ、水の導電率を大幅に向上させることができます。これが、雷雨や水源近くの電気機器を操作するときに、または水中または近くにいることが非常に危険である理由です。