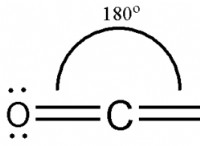
1。共有結合:
* 最も強いタイプの結合: これは、原子を分子内にまとめる主要な力です。
* 例:
* 炭素炭素結合 炭水化物、脂質、タンパク質、核酸の骨格において重要です。
* 炭素水素結合 すべての高分子に豊富です。
* 炭素酸素結合 炭水化物、脂質、核酸に存在します。
* 炭素窒素結合 タンパク質と核酸に不可欠です。
2。非共有結合:
これらの結合は共有結合よりも弱いが、生物学的分子の全体的な形状と相互作用に重要な役割を果たす。
* 水素結合:
* 構造に不可欠: これらの結合は、タンパク質と核酸(DNAとRNA)の形状に寄与します。
* 相互作用に関与: それらは、水の特性と、タンパク質 - タンパク質、タンパク質DNA、タンパク質水などの分子間の相互作用において重要な役割を果たします。
* イオン結合:
* 静電相互作用: これらの結合は、反対に帯電したイオン(正味の正または負の電荷を持つ原子)の間に形成されます。
* 構造における重要性: タンパク質と核酸の構造を維持するのに役立ちます。
* van der Waals Force:
* 弱いが重要: これらの力は、電子分布の一時的な変動から生じ、分子内の一時的な双極子を引き起こします。
* 相互作用を安定させる: それらは、分子の全体的な安定性とそれらの相互作用に貢献します。
* 疎水性相互作用:
* 非極性相互作用: これらの相互作用は、非極性分子(水と容易に相互作用しないもの)の傾向から生じます。
* タンパク質の折りたたみのキー: それらは、タンパク質の折りたたみと安定性に重要な役割を果たします。
要約:
*共有結合は、大きな生物学的分子のバックボーンを形成し、構造フレームワークを提供します。
*非共有結合、特に水素結合、イオン結合、疎水性相互作用は、他の分子との3次元の形状、安定性、および相互作用に不可欠です。
これらの結合は協力して、生物内で不可欠な機能を実行する複雑で動的な生物学的分子を作成します。