ホウ素は、周期表の 5 番目の元素です。これらのホウ素の事実には、一般的な情報と歴史とともに、化学的および物理的データが含まれています。

基本的なホウ素の事実
名前: ボロン
原子番号: 5
元素記号: B
グループ: 13
期間: 2
ブロック: p
エレメント ファミリー: メタロイド
原子質量: [10.806; 10.821] IUPAC ガイドライン。単一の値の場合は、10.811 を使用してください。
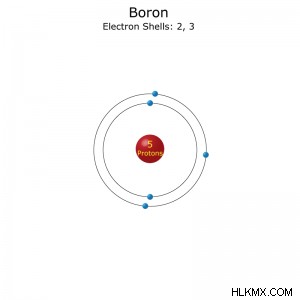
電子配置: [He]2s2p(短縮形) または 1s2s2p(フル)
発見: 1808 年に 3 人の科学者がホウ素を分離しました。
ホウ砂は何世紀にもわたって知られ、使用されてきました。セラミック釉薬や冶金で使用されましたが、誰もホウ砂から元素を分離しませんでした. 1808 年、Humphry Davy 卿はホウ砂溶液に電気分解を使用し、1 つの電極に茶色の塊が形成されることに気付きました。彼は後にカリウムを使用して、ホウ酸からホウ素を還元しました。フランスの海峡を越えて、Joseph Louis Gay-Lussac と Louis Jacques Thénard は、高温でホウ酸を鉄で還元することによってホウ素を分離しました。 1824 年にスウェーデンの化学者 Jöns Jakob Berzelius によってホウ素が元素として特定されました。
名前の由来: ホウ素という名前は、ホウ砂から抽出された鉱物に由来します。その名前はアラビア語の buraq に由来します 、石の通称。
天然同位体:
天然のホウ素は、B-10 と B-11 の 2 つの安定同位体で構成されています。 B-7 から B-17 までの範囲の実験室条件で、他に 11 の同位体が生成されています。
B
ホウ素 10 は 5 つの中性子を含む安定同位体です。天然ホウ素の 19.78% はホウ素-10 です。
B
ホウ素 11 は 6 個の中性子を含む安定同位体です。天然のホウ素の 80.22% はホウ素 11 です。

物理データ
密度: 2.34g/cm
融点: 2350 K (2077 ºC または 3771 ºF)
沸点: 4000 K (4273 ºC または 7232 ºF)
20ºC での状態: 固体
融合の熱: 50.2kJ/mol
気化熱: 508kJ/モル
モル熱容量: 11.087 J/mol・K
原子データ
原子半径: 0.90 Å (経験値)
共有半径: 0.84Å
ファン デル ワールス半径: 1.92Å
電子親和力: 26.989 kJ/mol
電気陰性度: (ポーリングスケール):2.04
1 イオン化エネルギー: 800.637 kJ/mol
2 イオン化エネルギー: 2427.069 kJ/mol
3 イオン化エネルギー: 3659.751 kJ/mol
4 イオン化エネルギー: 25025.905 kJ/mol
5 イオン化エネルギー: 32826.802 kJ/mol
一般的な酸化状態: +3 (一般的)、+2、+1、-5 (一般的でない)

楽しいホウ素の事実
- 純粋なホウ素は暗色の非晶質粉末です。
- ホウ素はメタロイドの中で最も高い融点を持っています。
- ホウ素はメタロイドの中で最も沸点が高い。
- ホウ素 10 同位体は、原子炉の中性子吸収体として使用され、緊急停止システムの一部です。
- ホウ素は、p 型半導体を作るためのドーパントとして半導体製造に使用されます。
- ホウ素は火炎試験で明るい緑色に燃えます。
- ボロンの緑色の炎の特性は花火に使用されています。
- 熱衝撃に対する耐性を高めるためにガラスにホウ素が添加されています。ほとんどの実験用ガラス器具はホウケイ酸ガラスでできています。
- ホウ素は超強力なネオジム磁石の主成分です。 Nd2 Fe14 B はこれらの磁石の化学式です。
- ホウ素は植物にとって必須の栄養元素です。人に対しては軽度の毒性があり、節足動物に対しては致命的です。ホウ酸は害虫駆除によく使用されます。
- 米国とトルコには、ホウ砂の最大の埋蔵量があります。
周期表の元素について学びましょう。