炭素 は周期表の 6 番目の元素です。これらのカーボン ファクトには、一般的な情報と歴史とともに、化学的および物理的データが含まれています。
楽しいカーボンの事実
- 炭素のグラファイトの同素体は、ダイヤモンドが最も硬い素材の 1 つであるのに対し、最も柔らかい素材の 1 つです。
- グラファイトは光沢のある黒く、ダイヤモンドは無色透明の固体であり、フラーレンと非晶質炭素はどちらも黒い煤のような粉末です。
- 炭素原子は鎖や環を形成し、水素原子で封印されて炭化水素と呼ばれる化合物を形成します。これらの化合物は、有機化学の非常に大きな部分を占めています。
- 炭素は、1,000 万を超えるさまざまな化合物を形成できる非金属です。
- 炭素は、すべての元素の中で最も高い昇華点を持っています。ダイヤモンドは約 3550 ºC で融解し、他の同素体は約 3800 ºC で昇華します。
- 純粋な炭素は、自然界に自由に存在する数少ない元素の 1 つです。
- 炭素は、宇宙で質量が 4 番目に多い元素です。
- 体重の 18% が炭素です。
- 断熱材としてグラファイトを使用。また、電気の良導体でもあります。
- 炭素 14 は、炭素年代測定法として知られるプロセスで、かつて生きていた物質の年代測定に使用されます。

炭素周期表セル
基本的な炭素の事実
名前: カーボン
原子番号: 6
元素記号: C
グループ: 14
期間: 2
ブロック: p
エレメント ファミリー: 非金属
原子質量: [12.0096; 12.0116] IUPAC ガイドライン。単一の値の場合は、12.011 を使用してください。
電子配置: [He]2s2p(短縮形) または 1s2s2p(フル)
発見: 炭素は有史以前から知られていた.
名前の由来: 炭素という名前は、ラテン語のcarboに由来します 、炭を意味します。
一般的な同素体: アモルファス、ダイヤモンド、フラーレン、グラフェン、グラファイト
天然同位体:
天然のホウ素は、2 つの安定同位体と 1 つの放射性同位体で構成されています。
C
炭素 12 は、6 個の中性子を含む安定同位体です。すべての天然炭素の約 99% は炭素 12 です。
C
炭素 13 は 7 中性子を含む安定同位体です。残りの天然炭素のほとんどは炭素 13 です。
C
炭素 13 は、8 個の中性子を含む放射性同位体です。炭素 14 は微量で自然に発生します。半減期は 5730 年で、β 崩壊によって N に崩壊します。
炭素 8 から炭素 22 までの 12 の人工放射性同位体が知られています。

カーボングラファイト (USGS)
物理データ
密度:
グラファイト:2.2 g/cmダイヤモンド:3.513 g/cm
昇華点: 3915 K (3642 °C, 6588 °F)
トリプルポイント: 10800 kPa で 4600 K
20ºC での状態: 固体
融合の熱: グラファイト:117 kJ/mol
モル熱容量:
グラファイト:8.517 J/mol·K
ダイヤモンド:6.155 J/mol·K
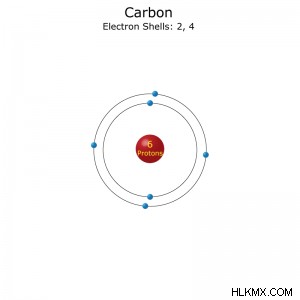
炭素原子の電子配置。
原子データ
原子半径: 1.70Å
共有半径: sp:0.77 Å
sp:0.73 Å
sp:0.69 Å
ファン デル ワールス半径: 1.70Å
電子親和力: 121.776 kJ/mol
電気陰性度: (ポーリングスケール):2.55
1 イオン化エネルギー: 1086.454 kJ/mol
2 イオン化エネルギー: 2352.631 kJ/mol
3 イオン化エネルギー: 4620.471 kJ/mol
4 イオン化エネルギー: 6222.716 kJ/mol
5 イオン化エネルギー: 37830.648 kJ/mol
6 イオン化エネルギー: 47277.174 kJ/mol
一般的な酸化状態: +4、-4 (共通)、+3、+2、+1、0、-1、-2、-3 (非共通)
周期表の元素の詳細をご覧ください。







