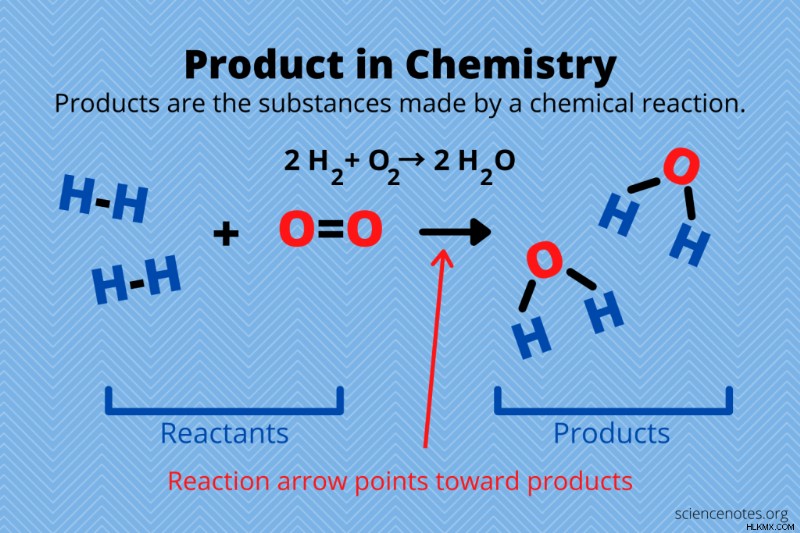
化学では、製品 化学反応から生じる化学種です。反応物は、高エネルギー遷移状態に入った後、生成物に変換されます。化学反応の生成物に含まれる原子の数と種類は、反応物に含まれる原子の数と種類と同じです。ただし、原子は互いに異なる化学結合を形成するため、生成物は反応物とは異なる化学的アイデンティティを持ち、物質の異なる状態になる可能性があります.
化学式での製品の識別
慣例により、生成物は化学式の右側にあります。反応矢印は製品を指しています。
A + B → C + D
A と B は反応物で、C と D は生成物です。
可逆反応では、矢印は両方向を指します。これは、矢印の両側の種が反応物と生成物の両方として機能することを意味します。
A + B ⇌ C + D
化学製品の例
以下は、化学における生成物、その反応物、およびバランスの取れた化学式の例です:
- 水、H2 Oは、水素と酸素の反応の生成物です。
2 H2 + O2 → 2 H2 ああ - 塩化銀、AgCl (s) は、水溶液中の銀カチオンと塩化物アニオン間の反応の生成物です。
Ag (aq) + Cl (aq) → AgCl (s) - 窒素ガスと水素ガスは、生成物としてアンモニアを形成する反応物質です。
N2 + 3 H2 → 2NH3 - プロパンを酸化すると、二酸化炭素と水が生成されます。
C3 H8 + 5 O2 → 3 CO2 + 4 H2 ああ
化学的および物理的変化における製品
化学変化と物理変化の主な違いは、化学変化では反応物が生成物とは異なりますが、物理変化では同じであるということです。言い換えれば、反応物は物質の状態を変えるかもしれませんが、物理的な変化では化学反応は起こりません.
たとえば、氷が溶けて水になることは、物理的変化の一例です。次の式はプロセスを表しています:
H2 O(s) → H2 O(l)
反応物と生成物の化学式は同じです。
反応生成物を予測する方法
化学反応の生成物を予測することは、ほとんどの場合、2 つの反応物間で可能な化学反応の種類を認識することです。たとえば、反応物が炭化水素と酸素である場合、生成物は二酸化炭素と水であると確信できます。分解反応により、単一の反応物が複数の生成物に分かれます。 2 つの元素が結合して、価電子殻を満たす比率で化合物を形成します。
ただし、製品の予測は条件にも依存します。条件によっては、反応物が異なる生成物を形成することがあります。たとえば、アンモニアは塩素と反応して、三塩化窒素と塩酸 (塩素が過剰の場合) または塩化アンモニウムと窒素 (アンモニアが過剰の場合) を形成します。
- NH3 + 3 Cl2 → NCl3 + 3 HCl
- 8 NH3 + 3 Cl2 → N2 +6 NH4 クリ
結局、予測の正確さは、主に経験と反応速度論の理解の問題です。
参考文献
- アトキンス、ピーター W.;フリオ・デ・パウラ (2006)。 物理化学 (第4版)。ワインハイム:Wiley-VCH. ISBN 978-3-527-31546-8.
- IUPAC (1997)。 "製品"。 化学用語集 (「ゴールドブック」)(第2版)。 Blackwell Scientific Publications:Oxford. ISBN 0-9678550-9-8. doi:10.1351/goldbook.P04861
- ウィバーグ、エゴン。 Wiberg、Nils。ホールマン、アーノルド・フレデリック(2001)。 無機化学 .アカデミックプレス。 ISBN 978-0-12-352651-9。