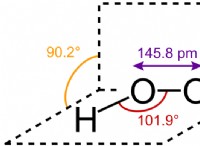
化合物とは、2 つ以上の成分からなる物質のことです。たとえば、水、食卓塩など
化合物には 2 種類あります
- 共有化合物
- イオン化合物
共有結合を含む化合物は、共有結合化合物として知られています。共有結合化合物は分子で構成されています。また、分子化合物としても知られています。
共有結合化合物は 2 つ以上の非金属元素から形成されるため、これは共有結合化合物を認識する方法の 1 つです。
共有結合には 2 つの基本的なタイプがあります
- 極性共有結合:電気陰性度の異なる 2 つの原子間で電子対を共有する共有結合です。例:HCl。
- 非極性共有結合:2 つの原子間で等しい電子を共有します。たとえば、C6H6、CO2、ガソリン、トルエン、一部の希ガスなど
いくつかの共有結合化合物の例
H2O – 水
炭水化物(砂糖とでんぷん)
O3 – オゾン
H2 – 水素
PCl3 – 三塩化リン
核酸 (DNA および RNA)
CH4 – メタン
CO2 – 二酸化炭素
O2 – 酸素
CH3CH2OH – エタノール
Cl2 – 塩素
NH3 – アンモニア
HCl – 塩化水素
タンパク質
脂質(脂肪)
共有結合の種類
共有結合には次の 3 種類があります:
- 一重共有結合
- 二重共有結合
- 三重共有結合
共有結合は、電子の共有によって原子間に形成されます。共有と言うとき、両方の原子が結合形成に寄与する必要があります。これは、各原子が少なくとも 1 つの電子を提供することを示しています。さらに、これは、共有結合には少なくとも 1 対または 2 つの電子が含まれることを示しています。
このような 1 対の電子が原子間で共有されるタイプの結合は、単共有結合と呼ばれます。 2 つの原子の間に 1 本の線を引くことで表されます。
単一共有結合化合物の例:
- 水素
- メタン
- 塩素
2 対の電子が原子間で共有されている場合、それは二重共有結合と呼ばれます。 2 つの原子の間に書かれた 2 つの線で表されます。
二重共有結合の例:
- 窒素
- 酸素
- カーボン
原子間で共有される 3 対の電子または単純に 6 つの電子は、三重共有結合と呼ばれます。
三重共有結合の例:
- 窒素ガス
- アセチレン
- シアン化物イオン
- 一酸化炭素
また、炭素は異なる元素と 3 つすべての共有結合を形成することができます。
単純な共有結合
単純な共有結合化合物に名前を付けるには、いくつかの規則があります。ルールは次のとおりです:
- 最初に最初の要素に名前を付け、その後で 2 番目の要素に名前を付けます。
- 最初の要素の原子が複数ある場合は、数値の接頭辞を使用する必要があります。その名前だけから簡単な共有結合化合物の化学式を決定できます。
- 一方、単純な共有結合化合物の名前を決定したい場合は、その化学式から決定できます。
- 一部の単純な共有化合物には、標準化された名前ではなく、一般的なフレーズや単語を使用します。
NH3:アンモニア
H2O:水
CH4:メタン
また、メタンは最も単純な有機化合物と言われています。
例外
分子が非金属のみで構成されている場合、それは共有結合化合物であると判断できます。ただし、重要な例外が 1 つあります。さらに、アンモニウム カチオン (NH4+) は陽性であるため、共有結合ではなく非金属とイオン結合を形成します。つまり、イオン性化合物です。
水素原子と窒素原子の間の結合は、正確な周期で共有結合です。したがって、硝酸アンモニウム塩化アンモニウムのような化合物には、イオン結合と共有結合が含まれます。
共有結合化合物の性質
- 気体 (CO2)、液体 (H2O)、柔らかい固体 (ろうそく) です。
- 融点が低い。
たとえば、氷は 0°C で溶けます。
例外:ダイヤモンドとシリカの分子は、融点が高いため例外です。
- 沸点が低い。たとえば、クロロホルムは 62°C、ベンゼンは 80.2°C で沸騰します。
- 電荷の非伝導体は、共有結合化合物の特性の 1 つです。液体または溶融物は電気を通しません。
- 共有化合物は熱の悪い伝導体です。
- 分子間の親和性は非常に低いです。
結論
この記事では、共有結合化合物とは何か、それらの紹介、共有結合化合物の例、共有結合化合物の種類、単純な共有結合化合物、例外、それらの特性など、いくつかのことについて説明しました。すべての側面について簡単に説明しました。 .最後に、学生は共有結合化合物の学習中にこの記事を参照して、理論の概念を明確にすることができます。