水素は周期表の最初の元素です。通常の状態では、無味無臭無色の気体です。二原子分子H2で構成され、記号Hで表されます。原子番号1の水素は、1つの電子と1つの陽子で構成されています。水素結合は、共有結合のいくつかの特性を共有する分子間で発生する静電双極子間接触として説明されます。水素結合は比較的強いため、相互作用パートナーの数が少なくなります。たとえば、化学的に (H2O) として表される水分子の場合、水素は電気陰性度の酸素原子に共有結合しています。
今日は、水素結合の概念、水素結合の例、その他の関連トピックについて詳しく説明します。それでは、さっそく始めましょう。
水素結合
水素結合は、水素原子と電気陰性度の高い原子の間の双極子間相互作用によって引き起こされる分子間力の一種である水素結合の定式化です。共有結合またはイオン結合と比較して、水素結合は一般的に弱いです。しかし、ファン・デル・ワールス軍よりは強い。専門家は、水素結合を弱い化学結合の一種として分類しました。
水素結合の例
水素結合の意味の例をいくつか示します –
水 – 電気陰性度の高い酸素原子は、水分子の水素原子と結合します。電子の共有ペアは酸素の原子に密接に引き付けられるため、分子の端は負になりますが、水素原子は正に見えます。
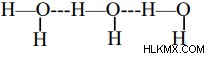
フッ化水素 – 水素結合において、フッ素は最高の電気陰性度を特徴とする最強の水素結合を形成します。
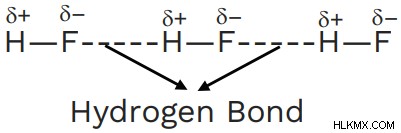
カルボン酸とアルコールの水素結合 – アルコールは、-OH 基を持つ有機分子と呼ばれます。一般に、水素原子を持つ分子が窒素または酸素に直接結合している場合。その後、水素結合が容易になります。
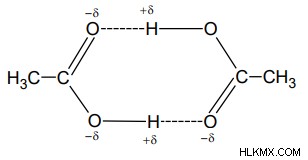
アンモニア中の水素結合 – 水素原子に結合した電気陰性原子窒素があります。
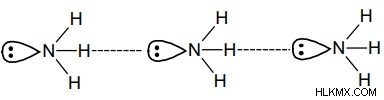
ポリマーの水素結合 – 天然および合成タンパク質が獲得する 3D 構造と特性を決定するために、水素結合は重要な要素です。また、亜麻や綿などの派生ポリマーとともにセルロース構造を定義する上でも重要な役割を果たします。
水素結合の種類と例
主に 2 つの重要なタイプの水素 (H) 結合とその例があります。これらには以下が含まれます –
-
分子間水素結合
同じ化合物または異なる化合物を持つ異なる分子間で水素結合が発生する場合、これらは分子間水素結合と呼ばれます。分子間水素結合の一般的な例には、アルコール、水、アンモニアなどの水素結合が含まれます。
例:
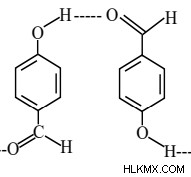
-
分子内水素結合
分子内水素結合は、主に分子内のみで起こる水素結合として説明できます。このタイプの水素結合は、2 つのグループを持つ化合物で発生します。 2 つのグループのうち、1 つのグループには水素原子があり、別のグループには電気陰性度の高い原子があります。
例:
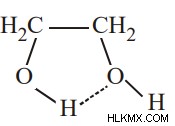
水素結合の条件
水素原子が電気陰性度の高い原子に密接に結合している分子では、電子の共有部分が引き付けられます。その結果、分子の端はわずかにマイナスになり、もう一方の端はプラスになります。両端が互いに引き付け合い、弱い結合が形成されます。この結合は水素結合と呼ばれます。水素結合の 2 つの主な条件は次のとおりです。
各分子には、水素原子に接続された非常に電気陰性度の原子が必要です。電気陰性度が高いほど、分子の分極が高くなります。
電気陰性原子のサイズは小さくする必要があります。サイズが小さいほど、静電引力は大きくなります。
なぜ水素結合化合物は高い融点と高い沸点を持っているのですか?
水素結合化合物は、一般に沸点と融点が高くなります。水素結合化合物のこれらの高温は、これらの結合を切断するために必要なより多くのエネルギーの原因となります。
室温では、H2O は液体です。ただし、H2S、H2Se、および H2Te は気体の状態で見つかります。水素結合は水分子の結合を生じさせるため、他の化学物質と比較すると沸点と融点が高くなります。
NH3 には水素結合があるため。ただし、PH3 には水素結合はありません。アンモニアは沸点が高いです。
エタノールには水素結合があるため、沸点はジエチル エーテルよりも高くなります。
結論
これで、水素結合の例の話題は終わりです。水素結合は、水素原子と非常に電気陰性度の高い原子との間の双極子間相互作用によって生じる分子間引力の特別なクラスである水素結合を形成するプロセスとして説明できます。それは主に電気陰性と水素原子の間で発生します。
専門家は、水素結合を弱い化学結合の一種として分類しています。水素結合の意味の一般的な例のいくつかは、フッ化水素の水素結合、水中の水素結合、アンモニアの水素結合、ポリマーの水素結合などであり、詳細に説明しました.さらに、分子間水素結合と分子内水素結合の 2 つの主要な部分に分類されます。後半では、水素結合の性質と条件について簡単に触れました。これが水素結合の概念をよりよく理解するのに役立つことを願っています.







