無水アンモニアは無機化学の溶媒として使用されるため、無水アンモニアの作り方を知ることが重要になります。ほとんどの化学反応には適切な溶媒が必要です。水は、無機化学で主に使用される溶媒です。有機化学では有機溶媒が使われます。水を使用することには多くの利点がありますが、次の理由により、水以外の溶媒の使用が開発されました。
• 水は還元されて水素が発生するため、強力な還元剤が関与する反応は水中では実行できません。
• 水は一部の化合物を加水分解できます。
• 特別な装置がない限り、高温 (>100 °C) での反応は実行できません。
アンモニアは、最も広く使用されている非水溶媒の 1 つで、無水アンモニアと呼ばれます。沸点が高く、室温以下で沸騰します。
| プロパティ | アンモニア | 水 |
| 融点 沸点 融解熱/ kJ mol 気化熱/ kJ・mol 密度/kg m | 195.41 239.80 5.66 23.35
667 @ 240.15 K | 273.15 373.15 6.00 40.72
960 @ 373.15 K |
無水アンモニアを作る
アンモニアは気道を刺激します。したがって、アンモニアの準備と作業はヒューム カップボードで行う必要があります。
方法 1:
- 1~2 g の塩化アンモニウムと 1~2 g の消石灰(水酸化カルシウム - Ca(OH)2 ).
- 混合物を試験管に移し、ベントガス放電管を収容する栓で閉じます。
- 試験管を混合物で加熱します。
- 濃塩酸で湿らせたリトマス試験紙をガス放電管の端に持っていきます。
方法 2:
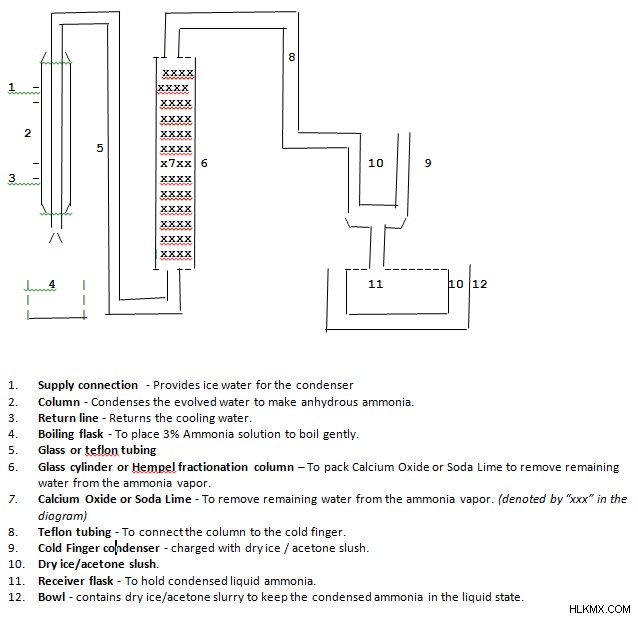
手順:
• まず、塩化アンモニウム/水溶液をフラスコに入れ、氷/塩浴を使用して 0 C まで冷やします。
• 次に等規定量の塩化ナトリウムを加えて、塩化アンモニウムをアンモニア塩に変換します。 (アンモニアの濃度が 40% 未満になるように十分な量の水を追加する必要があります。0 C で約 47% 飽和するため)
• 次に、フラスコの内容物を穏やかに沸騰させて、アンモニアをガスとして放出します。その過程で発生する水蒸気がやって来て、凝縮してフラスコに戻ります。沸騰プロセスは、アンモニアが放出されなくなるまで続きます。
アンモニアガスの放出が終わったら、次の蒸留のために沸騰フラスコを再充填することができます.
• 収集したアンモニアをセットアップから切り離してすぐに使用し、液体アンモニアを必要とする反応をその場で実行します (例:バーチ還元)。
• 回収されたアンモニアは無水で、凝縮器内の水は CaO ドライヤーで除去できます。コールドフィンガーと接触して氷を形成することで、さらに取り除くことができます.
無水アンモニアの作り方 – まとめ
無水アンモニアは、特徴的な刺激臭のある無色の気体です。腐食性ガスで、水によく溶けます。無水アンモニアは、広く使用されている非水性溶媒です。無水アンモニアの小規模生産に利用できるいくつかの方法があります。大規模生産では、非常に高い温度と圧力で水素と窒素を使用して生産されます。