分子から 2 つ以上の原子が取り除かれる有機反応は、脱離反応と呼ばれます。除去は、金属、酸、または塩基の作用によって、または高温まで加熱することによっても行われます。脱離反応では、炭素原子間の単結合が二重結合または三重結合に変換されます。言い換えれば、飽和化合物は不飽和化合物に変換されます。
脱離反応は、分子を離れる原子の種類に基づいて分類されます。たとえば、2 つの水素原子の除去は、脱水素化と呼ばれます。 1 つの水素原子と 2 つの酸素原子 (1 つの水分子) の除去は、脱水または β 脱離と呼ばれます。 1 個の水素原子と 1 個のハロゲン原子の除去は、脱ハロゲン化水素と呼ばれます。 2 つのハロゲンの除去は、脱ハロゲン化と呼ばれます。反応速度論に応じて、除去反応も E1 および E2 反応として分類されます。
脱離反応のメカニズム
除去反応には、次の基本的なメカニズムが含まれます:
プロトンの脱離
2 つの炭素原子間のパイ結合 (C=C) の形成
脱退グループとの絆を断ち切る
E1 反応
単分子脱離反応は E1 反応と呼ばれます。
この反応の速度は k [R-LG] であり、分子種が分解されるステップが反応の速度を決定することを意味します。
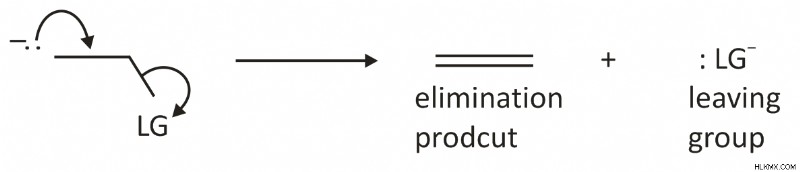
E1 反応の最初のステップでは、脱離基 (LG) が失われ、炭素原子に正電荷が形成されます (カルボカチオン中間体)。 .これは次のように説明できます:
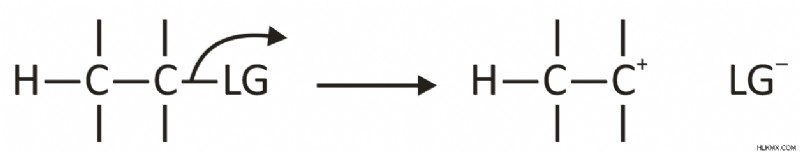
2 番目のステップでは、H+ イオンが塩基 (B) に失われ、パイ結合が形成されます。これは次のように説明できます:
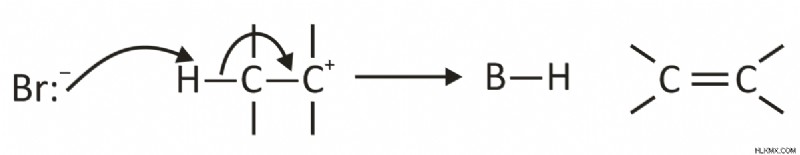
反応速度は、脱離基が有機化合物によって失われて中間体を形成するステップによって決まります。
離脱基の性質に基づいて、反応が速い場合と遅い場合があります。これは、レート決定ステップが脱退グループの損失に基づいているためです。
第 2 段階は反応速度に影響しないため、塩基 (B) の性質は重要ではありません。
E2 反応
二分子脱離反応は E2 反応と呼ばれます。
この反応の速度は、k[B][R-LG] と書くことができます。これは、塩基 ( B) と有機基板 (R LG) は、反応の律速段階です。
この反応では、脱離基の除去、塩基によるプロトン (H+) の除去、およびパイ結合の形成が同時に行われます。
E2 反応は次のように説明できます:
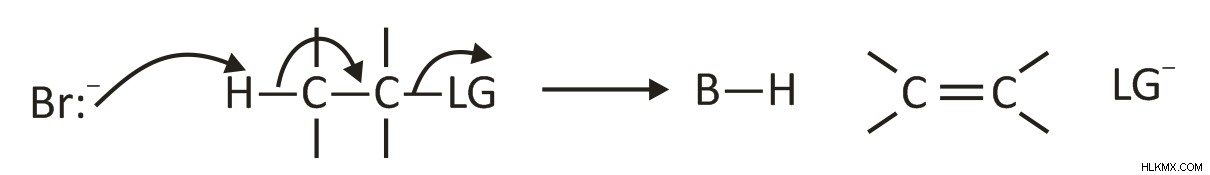
sp3 混成炭素原子は sp2 混成に変わります。
脱離基の性質は、反応の律速段階で脱離するため、反応速度に影響します。
脱離基が良すぎると、E2 反応が E1 反応に変わることがあります。
より反応性の高い塩基は、E2 反応の速度に有利に働きます。
E1CB 反応
単分子 (E1) 共役塩基 (CB) 反応は、E1CB 反応と呼ばれます。
これは 2 段階の反応です。
最初のステップでは、水素が塩基 (B) によって除去され、アルコキシド アニオンが形成されます。言い換えれば、最初のステップでは、陰イオンを形成するための脱プロトン化が行われます。最初のステップは次のように説明できます:

2 番目のステップでは、脱離基 (LG) が除去され、電子対によって共役塩基から置換されると、パイ結合が形成されます (したがって、用語 CB) を次のように:
不十分な脱離基は反応を遅くするため、反応の第 2 段階がその速度を決定します。
結論
分子から 2 つ以上の原子が除去される有機反応は、脱離反応と呼ばれます。脱離反応のメカニズムには、プロトンの除去、パイ結合の形成、脱離基の除去が含まれます。
脱離反応には、E1、E2、E1CB の 3 種類があります。 E1 反応では、脱離基が除去され、続いて塩基による水素イオンの除去が行われ、パイ結合が形成されます。 E2 反応では、脱離基の除去、塩基による H+ イオンの除去、および pi 結合の形成が同時に行われます。 E1CB 反応では、脱離基 (LG) が除去され、共役塩基から電子対によって置換されると、水素イオンが塩基によって除去され、続いて pi 結合が形成されます。