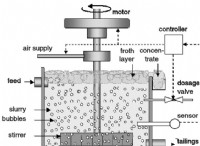
共沸蒸留では、分離プロセスを使用して、共沸混合物のすべての成分を分離します。共沸混合物は、通常、単純な蒸留では区別できない 2 つ以上の流体を含んでいます。これらの混合物を加熱することによって生成される煙には、組み合わせ自体と同じ割合の液体が含まれています。その結果、共沸蒸留は、共沸混合物を溶解するための特定の手順を含む特殊な蒸留です。共沸混合物を分解するための最も一般的なアプローチは、材料分離試薬を使用して、いくつかの共沸成分間の分子接続を変更することです。物質分離剤を添加すると、共沸混合物中の化学物質の全体的な作用が変化します。その結果、共沸混合物全体の全体的な相対揮発性が変化します。
物質分離剤
ベンゼンなどの物質分離試薬を水とエタノールの組み合わせに加えると、分子の結合が変化し、共沸が解消されます。新しい成分が液体の状態で導入されると、通常、さまざまな方法で複数の化学物質の活性化係数が変化し、混合物の比較的揮発性が変化します。他の要素を含めると、Raoult のルールを超えたより高い逸脱は平滑化される傾向があり、相対的なボラティリティにかなりの変動が生じます。
最近追加されたコンポーネントの揮発性は、共沸蒸留内の混合物のようなものです。極性の変化に基づいて、1 つまたは複数の成分を含む独自の共沸混合物が作成されます。エントレーナーは、入力に複数の成分を含む共沸混合物を生成するために使用される化学分離剤です。デカンテーション、蒸留、またはその他の分離手順を使用して余分なエントレーナーを収集します。これは、既存のカラムの上部に向かって復元する必要があります。
水エタノール蒸留
共沸蒸留でエタノールと水の混合物を蒸発させるには、具体的な例が必要です。これを行うために、共沸混合物が共沸蒸留されやすい最終段階に供給されます。ベンゼン、シクロヘキサン、ヘキサン、ペンタン、イソオクタン、アセチレン、ジエチル エーテル、およびヘプタンは、この方法で利用される共留剤の一部です。ベンゼンとシクロヘキサンは、最も一般的に使用される化学物質です。
残念なことに、ベンゼンには有害な性質があるため、その使用は減少しています。エタノールを脱水する最も一般的な方法でしたが、毒性が高く、それに関連する資本コストが高いため、支持されなくなりました。ベンゼンの代わりにトルエンを使用することは、エタノールと水の共沸混合物を分解するための害が少なく、有利なアプローチであることが証明されています.
抽出蒸留と共沸蒸留の違い:違いは何ですか?
抽出蒸留と共沸蒸留の基本的な違いは、混合物の分離プロセスにあるようです。すべての組み合わせには、抽出蒸留中に共沸混合物を形成しない特定の分離溶媒が必要です。この点を考慮すると、抽出蒸留は共沸蒸留よりも単純なアプローチです。
共沸混合物の分解
最小沸騰共沸混合物と最大沸騰共沸混合物は、2 つの主要な種類です。最小沸点共沸混合物はラウルの法則から正に逸脱しますが、最大沸点共沸混合物は負に逸脱します。最低沸点共沸混合物は比較的低い温度で沸騰しますが、最高沸点共沸混合物は極端な温度で沸騰します。蒸留技術は、低温で沸騰する共沸混合物の揮発性成分を昇華させません。共沸混合物を分割すると、通常は純粋な物質が得られます。このアプローチは、蒸留に依存しない分離技術を提供します。モレキュラーシーブの使用には、一般的に異なる方法が含まれます。
結論
共沸蒸留は、共沸混合物を形成するすべての成分を分離する方法です。共沸混合物の沸点は、その成分の沸点より高くても低くてもよく、単純な蒸留では溶液の成分を区別できないため、共沸混合物の不確実性を修正するために 3 番目の要素が使用されます。圧力が使用されます。共沸蒸留の一般的な歴史的例は、エタノールと水の混合物を脱水する際の使用です。ベンゼン、ヘキサン、シクロヘキサン、イソオクタン、アセトンなどは、この手順で使用される溶媒の一部です。