主な違い - 蒸気圧と沸点
気化と沸騰は、液体または固体の相変化を表すために使用される 2 つの用語です。気化とは、液体または固体が蒸気になる相変化です。沸騰は、液体から蒸気への相変化を引き起こします。気化により、密閉系の蒸気圧が上昇します。沸点は、液体が気化する温度です。これら 2 つの用語は互いに関連していますが、両者には違いがあります。蒸気圧と沸点の主な違いは、蒸気圧は圧力の測定値であることです。 一方、沸点は温度の測定値です。
対象となる主な分野
1.蒸気圧とは
– 定義、条件、特徴
2.沸点とは
– 定義、特徴
3.蒸気圧と沸点の違いは何ですか
– 主な違いの比較
重要な用語:蒸気、沸点、蒸気圧、運動エネルギー、温度、大気圧 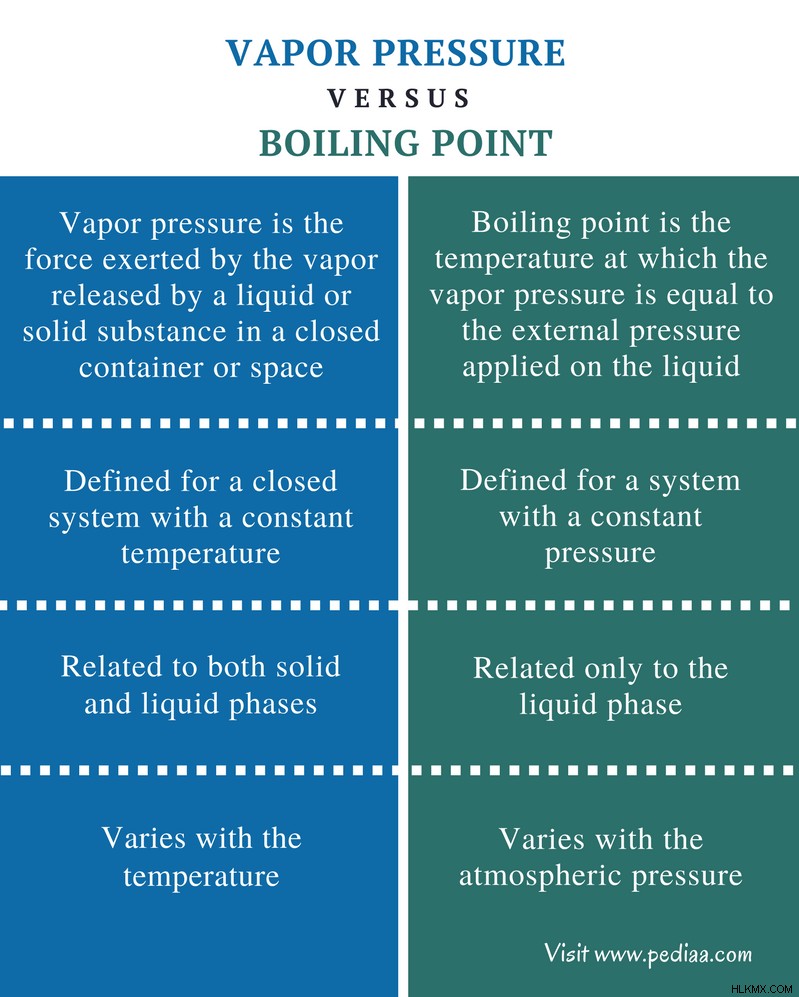
蒸気圧とは?
蒸気圧は、蒸気によって加えられる力として定義できます。蒸気圧を発生させるには、蒸気が次の条件を満たしている必要があります。
- 蒸気は液相または固相と平衡状態にある必要があります。
- 蒸気は一定の温度でなければなりません。
- 蒸気とその凝縮形態の両方が閉鎖系に存在する必要があります。
蒸気圧は、分子が液体または固体から逃げたいという欲求に関係しています。したがって、常温で蒸気圧の高い物質は揮発性と考えられます。温度が一定に保たれている限り、蒸気圧も一定に保たれます。しかし、温度が上昇すると、液体分子のキネシス (運動エネルギー) が増加し、液体からより多くの分子が放出されます。その結果、液体分子の蒸気への遷移が増加します。したがって、蒸気圧も増加します。ある温度では、蒸気圧は液体または固体にかかる外圧と等しくなります。この温度は液体の沸点と呼ばれます。

図 1:蒸気圧
沸点とは?
沸点は、液体が沸騰する温度です。言い換えれば、液体の蒸気圧が、周囲の環境によって液体に加えられる外圧と等しくなる温度です。
液体の沸点は大気圧によって異なります。したがって、特定の液体の沸点の値は常に一定ではありません。気圧は標高によって変化します。たとえば、大気圧が 1 気圧の場合、水は通常 100 ℃ で沸騰します。しかし、標高が高い場所では、水はより低い温度で沸騰します。これは、液体が沸騰するには蒸気圧が大気圧と等しくなければならないためです。高地では気圧が低いため、熱エネルギー (温度) が低くても上記の基準を満たすのに十分です。
沸点以下の温度でも、液体分子は蒸発と呼ばれるプロセスにより蒸気になります。蒸発とは、液体の表面にある液体分子が逃げることです。これらの分子は、液体中の他の分子にゆるく結合しているだけです。したがって、それらは他の分子から容易に分離し、蒸気として液体から逃げることができます。しかし、沸騰中は、液体中のどこにでもある分子が液体から逃げることができます。

図 02:ケトルの開口部から出る水蒸気
蒸気圧と沸点の違い
定義
蒸気圧: 蒸気圧は、密閉された容器または空間内の液体または固体物質によって放出される蒸気によって加えられる力です.
沸点: 沸点は、蒸気圧が液体にかかる外圧と等しくなる温度です。
特定の条件
蒸気圧: 蒸気圧は、温度が一定の閉鎖系に対して定義されます。
沸点: 沸点は、圧力が一定のシステムに対して定義されます。
物理的状態
蒸気圧: 蒸気圧は、固相と液相の両方に関連しています。
沸点: 沸点は液相のみに関係します。
バリエーション
蒸気圧: 蒸気圧は温度によって変化します。
沸点: 沸点は大気圧によって変化します。
結論
蒸気圧と沸点は、物理化学でよく使用される 2 つの関連用語です。蒸気圧は沸点に関係していますが、それらは異なる特性を持っています。蒸気圧と沸点の主な違いは、蒸気圧は圧力の測定値であるのに対し、沸点は温度の測定値であることです.







