主な違い - 複塩と複合塩
化学では、塩は陽イオンと陰イオンから構成されるイオン化合物です。陽イオンは正に帯電した化学種であり、陰イオンは負に帯電した化学種です。したがって、塩は中性化合物です。陽イオンと陰イオンが相互作用すると、塩全体の電荷がゼロになるように結合します。陽イオンと陰イオンは、イオン結合を介して結合します。複塩と錯塩は、化学で見られる 2 種類の塩です。複塩と錯塩の主な違いは、複塩は 2 つの塩化合物の組み合わせであるのに対し、錯塩は 1 つ以上の錯イオンで構成される分子構造です。
対象となる主な分野
1.ダブルソルトとは
– 定義、プロパティ、および例
2. 複合塩とは
– 定義、プロパティ、および例
3. 複塩と複合塩の違いは何ですか
– 主な違いの比較
重要な用語:陰イオン、陽イオン、錯塩、複塩、イオン性化合物、塩 
ダブルソルトとは
複塩は、2 つの異なる塩化合物を組み合わせて調製した化合物です。したがって、複塩は複数の陰イオンと陽イオンで構成されています。複塩は、塩化合物を同じ液体に溶解し、続いて規則的なパターンで結晶化することによって調製されます。

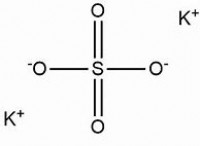
図 1:硫酸アンモニウム鉄 (II) は複塩です
水に溶解すると、複塩はすべてのイオンに完全に解離します。複塩の水溶液は、最初の2つの塩化合物にあった陽イオンと陰イオンで構成されています。したがって、この解離により、水溶液中に単純なイオンが生成されます。
複塩は水中で完全に解離するため、水に溶かすことで簡単に分析できます。ただし、複塩を調製する場合は、成分(2つの塩)を等モル比で混合する必要があります。つまり、同量のモルを混合する必要があります。そうしないと、均一で規則的な格子を取得できません。
複塩の例としては、ミョウバン、タットン塩、酒石酸カリウム ナトリウム、ブロムライトなどがあります。複塩結晶の特性は、最初に使用された塩の特性とは異なります。複塩の調製
複合塩とは
錯塩は、配位子との配位結合を持つ中央の金属原子から構成される化合物です。これは配位化合物とも呼ばれます。この化合物は構造が複雑で、陽イオンと陰イオンが結合しているため、錯塩と呼ばれています。
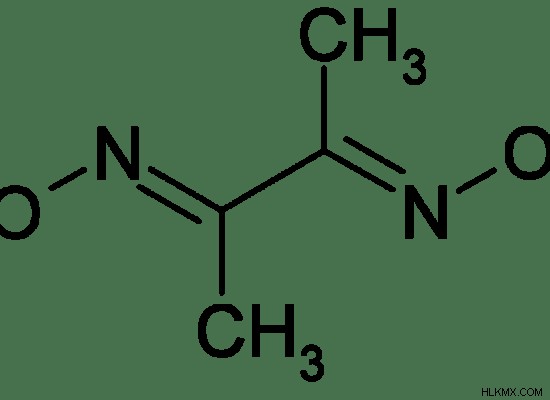
図 2:ジメチルグリオキシムは錯塩です
錯塩は、水に加えられたときに完全に解離してイオンになるわけではありません。代わりに、それらは複雑な構造のままです。この複合体の形成は、金属イオンのキレート化に役立ちます。ここで、金属イオンは配位結合を介して配位子と呼ばれる化学種に結合しているため、金属イオンは反応混合物で起こる他の化学反応には利用できません。これは、特定の金属イオンによる干渉を除去する必要がある化学反応において重要です。
ただし、錯塩は単純イオンを生成しないため、錯塩を水に溶かして分析することはできません。錯塩は、化学量論比で 2 つの異なる塩を混合することによって調製されます。その後、適切な量の配位子が金属イオンと結合します。
複塩と複合塩の違い
定義
二重塩: 複塩は、2 つの異なる塩化合物の組み合わせによって調製される化合物です。
複合塩 : 錯塩は、配位子との配位結合を持つ中心金属原子から構成される化合物です。
解離
ダブルソルト: 複塩は水中で完全にイオンに解離します。
複合塩 : 錯塩は水中でそのイオンに完全には解離しません。
発生するイオン
ダブルソルト: 複塩は、水に加えると単純イオンになります。
複合塩 : 錯塩は単純なイオンを与えません.
分析
ダブルソルト: 複塩は、水溶液中に存在するイオンを測定することで簡単に分析できます。
複合塩 : 錯塩は、水溶液中のイオンを測定するだけでは簡単に分析できません。
結論
塩は、基本的に陰イオンと陽イオンで構成されています。したがって、複塩や錯塩にも陽イオンと陰イオンが含まれています。どちらも塩と呼ばれていますが、調製方法や化学的挙動によって異なります。しかし、複塩と錯塩の主な違いは、複塩は 2 つの塩化合物の組み合わせであるのに対し、錯塩は 1 つ以上の錯イオンから構成される分子構造であることです。