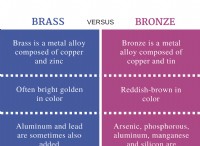
$$ cu + 4hno_3 \ rightarrow cu(no_3)_2 + 2no_2 + 2h_2o $$
方程式の化学量論から、1 molのCuが4 molのHNO3と反応することがわかります。したがって、2.0 molのHNO3と反応するには、次のことが必要です。
$$ 2.0 \ text {mol hno} _3 \ times \ frac {1 \ text {mol cu}} {4 \ text {mol hno} _3} =0.50 \ text {mol cu} $$
Cuのモル質量は63.55 g/molです。したがって、必要なCuの質量は次のとおりです。
$$ 0.50 \ text {mol cu} \ times 63.55 \ text {g/mol} =\ boxed {31.78 \ text {g cu}} $$