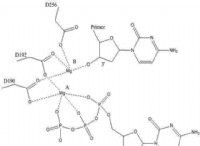
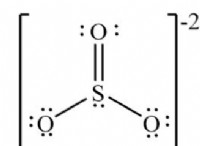
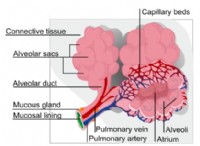
溶媒和のプロセスは、次の手順の観点から理解できます。
1.イオン化合物は、その構成イオンに解離します。
2。溶媒分子はイオンを囲み、その周りに水和シェルを形成します。
3.水和シェルはイオンを安定させ、再結合しないようにします。
溶媒和の強さは、次の要因に依存します。
* 溶媒の極性。 水などの極性溶媒には、誘電率が高いため、電荷は簡単に分離できます。これにより、イオン化合物の溶媒が良好になります。
* イオンの電荷。 イオンが高く帯電しているほど、溶媒和が強くなります。これは、イオンがより高く帯電しているほど、極性が高いためです。
* イオンのサイズ イオンが小さいほど、溶媒和が強くなります。これは、イオンが小さいほど、溶媒分子に囲まれやすいためです。
溶媒和イオンは、多くの化学反応において重要な役割を果たします。それらは多くの水性反応の反応物であり、反応を触媒するためにも使用することができます。