1。共有結合:
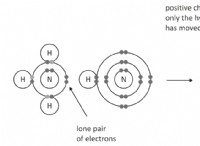
- ダイヤモンドは、ダイヤモンドの立方体構造として知られる非常に硬くて密集した結晶構造に配置された炭素原子で完全に構成されています。
- ダイヤモンドの各炭素原子は、4つの隣接する炭素原子と共有結合を形成し、非常に安定した電子構成を作成します。
- 共有結合には、原子間の電子の共有が含まれ、炭素原子をしっかりと保持する強力な原子間力をもたらします。
2。四面体結合配置:
- ダイヤモンド立方体の構造では、各炭素原子は四面体の中心にあり、角に他の4つの炭素原子に囲まれています。
- この四面体の配置は、電子の対称的で均一な分布をもたらし、例外的な強度と安定性をもたらします。
3。強力な炭素炭素結合:
- ダイヤモンド内の炭素原子間の共有結合は非常に強く、1モルあたり348キロジュールの結合エネルギーがあります。
- この高い結合エネルギーは、炭素の高い電気陰性度から生じます。これにより、電子が原子間で均等に共有され、強い引力と他の元素と反応する傾向が低くなります。
4。欠陥の欠如:
- ダイヤモンドの純度は、その硬度と非反応性において重要な役割を果たします。
- 空室、不純物、脱臼などの欠陥が少ないダイヤモンドは、より堅牢で均一な結晶構造を持ち、変形や化学反応により耐性があります。
5。高い熱伝導率:
- ダイヤモンドには非常に高い熱伝導率があり、これにより熱を効率的に消散させることができます。
- ダイヤモンドの強力な共有結合は、結晶格子全体の熱の急速な移動を促進し、局所的な加熱を防ぎ、ダイヤモンドの構造を保護します。
これらのユニークな構造的特徴と強力な共有結合の結果として、ダイヤモンドは顕著な硬度を持ち、地球上で最も硬い自然材料になります。また、化学反応や変換にも耐性があり、ほとんどの環境では非常に非反応性があり、反応性がありません。