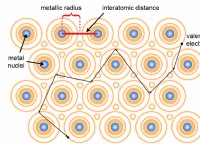
原子の正式な電荷を計算するには、最初に原子が持っている価電子の数を知る必要があります。次に、原子が他の原子に結合した電子の数を知る必要があります。最後に、原子が持っている電子の唯一のペアの数を知る必要があります。
原子の正式な電荷は次のように計算されます。
正式な電荷=(価電子の数) - (結合電子の数) - (電子の孤立ペアの数)
GEF6 2-の場合、正式な料金は次のとおりです。
GE:4価電子-6結合電子-0電子の孤立ペア=+2正式な電荷
F:7価電子-1結合電子-3孤立電子のペア=-1正式な電荷
分子内のすべての原子の正式な電荷の合計は、分子の全体的な電荷に等しくなければなりません。この場合、GEF6 2-の全体的な電荷は-2であるため、GEおよびF原子の正式な電荷の合計も-2でなければなりません。