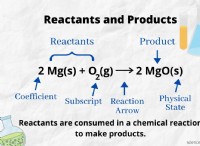
1。反応物と生成物
* 反応物: スクロース(c₁₂h₂₂o₁₁)と酸素(o₂)
* 製品: 二酸化炭素(co₂)と水(h₂o)
2。不均衡な方程式
c₁₂h₂₂o₁₁ +o₂→co₂ +h₂o
3。検査によるバランス
* 炭素: 左側には12個の炭素原子があり、右側に1本の炭素原子があります。 CO₂を12倍にします。
* 水素: 左側には22の水素原子、右側に2つの水素原子があります。 H₂Oを11を掛けます。
* 酸素: ここで、両側に酸素原子を数えます。左側に11個、右側に35個あります。 酸素のバランスをとるために、O₂の前に12の係数を追加します。
4。バランスの取れた方程式
c₁₂h₂₂o₁₁ + 12o₂→12co₂ + 11h₂o
重要な注意: この方程式は、通常、高温で発生するスクロースの完全な燃焼を表しています。生物系では、酵素を含む一連のステップを通じてショ糖酸化が発生します。