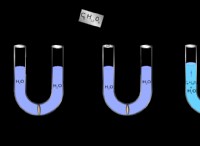
基本
* 融点: 純水氷は0°C(32°F)で溶けます。
* 凍結点うつ病: 塩または砂糖を水に加えると、凍結点が低下します。これは、氷が0°Cより低い温度で溶けることを意味します。
塩
* メカニズム: 塩(NaCl)は水に溶け、凍結点が低い溶液を作成します。これは、塩イオンが氷の結晶構造の形成を破壊するためです。
* 温度効果: 氷が寒いほど、それほど効果は低い塩が溶けています。これは、塩を溶かすために利用できる水が少ないためです。
* 例: 塩は、凍結に近い日よりも、寒い冬の日に氷を溶かすのにはるかに効果的です。
砂糖
* メカニズム: 砂糖(スクロース)も水の凍結点を低下させますが、塩よりも効果が低くなります。砂糖分子は、溶解している間、塩のようにイオンに解離しないでください。これは、氷の構造をあまり効果的ではないことを意味します。
* 温度効果: 塩と同様に、砂糖は寒い温度で氷を溶かすのにあまり効果的ではありません。
* 例: 砂糖は氷を溶かすのに役立ちますが、同じ効果を達成するには塩よりもかなり大きな量が必要です。
要約
* 塩と砂糖の両方が水の凍結点を下げ、氷が低い温度で溶けます。
* 塩は溶けた氷の砂糖よりも効果的です。
* 温度が低下すると塩と砂糖の両方の有効性が低下します。
実際のアプリケーション
* 道路の脱アイシング: 塩は、道路や通路で氷を溶かすために使用されます。
* アイスクリームの製造: 砂糖は、アイスクリーム混合物の凍結点を下げるために使用され、硬くなりすぎないようにします。
* ホーム実験: 単純な実験で氷の融解に対する塩と砂糖の効果を簡単に示すことができます。