* 燃料(還元剤): 木材、プロパン、ガソリンなどの燃料には、比較的低い結合エネルギーを持つ化学結合が含まれています。 これは、これらの結合の電子があまりしっかりと保持されていないことを意味します。
* 酸素(酸化剤): 酸素ガス(O2)は、電子に対して強い親和性を持っています。
* 反応: 燃料と酸素が接触すると、酸素は電子を燃料から「引き離す」。 この電子の伝達は、酸化還元反応の心臓です。
簡単な例:
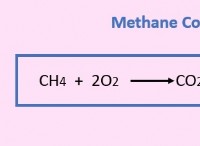
* 燃料: メタン(CH4)
* 酸素: 酸素(O2)
反応: CH4 + 2O2-> CO2 + 2H2O
* 酸化: メタン(CH4)は電子を失い、二酸化炭素(CO2)に酸化します。
* 削減: 酸素(O2)は電子を獲得し、水(H2O)に還元されます。
キーポイント:
* エネルギー放出: 電子の移動は、熱と光の形でエネルギーを放出するため、燃料を燃やします。
* 燃焼: これは、燃焼として知られる酸化還元反応の一種です。
* 重要性: 燃焼は、エネルギー生産、輸送、および現代生活の他の多くの側面において重要な役割を果たしています。
その他の一般的な例:
* 鉄の錆び: 鉄(Fe)は、酸素(O2)と反応して、一般に錆として知られている酸化鉄(Fe2O3)を形成します。
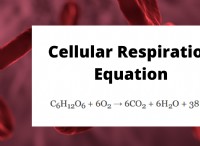
* 呼吸: 生物はグルコース(C6H12O6)を燃料および酸素(O2)として使用して、二酸化炭素(CO2)と水(H2O)を生成します。このプロセスは、エネルギーを放出して体を動かす複雑な酸化還元反応です。
* バッテリー操作: バッテリーは、酸化還元反応に依存して電力を生成します。
酸化削減反応の特定の例や側面について詳しく知りたい場合はお知らせください!