* 蒸気圧 液相と平衡状態の液体の蒸気によって加えられる圧力です。
* 衝突特性 そのアイデンティティではなく、溶質粒子の濃度に依存する溶液の特性です。 蒸気圧を下げることは、これらの衝突特性の1つです。
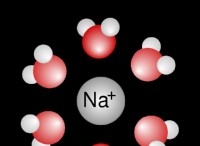
* 塩化ナトリウム(NaCl) 水に溶解すると、2つのイオン(Na+およびCl-)に解離するイオン化合物です。これは、1 mのNaCl溶液が、糖のような非イオン性化合物の溶液よりも溶解した粒子の濃度が高いことを意味します。
それがどのように機能するか:
* 純水: 水分子は、蒸気相に逃げる傾向が比較的高いため、蒸気圧が高くなります。
* 水溶液溶液: 溶存イオン(Na+およびCl-)は水分子と相互作用し、水分子が蒸気相に逃げるのが難しくなります。これにより、蒸気圧が減少します。
要約: 溶液中の溶存塩化ナトリウムイオンの存在は、純水と比較して蒸気圧を下げます。これは、蒸気圧力低下として知られる衝突特性の直接的な結果です。