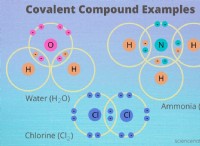
* 周期表の場所: ナトリウムはグループ1(アルカリ金属)に見られる金属であり、塩素はグループ17(ハロゲン)に見られる非金属です。
* 反応性: ナトリウムは非常に反応性があり、1つの電子を容易に失い、陽性イオン(Na+)を形成します。塩素も反応性があり、1つの電子を容易に獲得して負のイオン(Cl-)を形成します。
* 物理状態: ナトリウムは、室温で柔らかく銀色の金属です。塩素は黄緑色の刺激的なガスです。
* 反応: ナトリウムは水と激しく反応し、水素ガスを放出します。塩素は金属と反応して塩を形成することができます。
* 外観: 塩素は緑がかった黄色のガスですが、ナトリウムは光沢があり金属です。
それらが似ている唯一の方法は、両方とも容易にイオンを形成することです。これは、塩化ナトリウム(NaCl) - テーブル塩を形成するために結合するときのイオン結合の基礎です。