1。反応物とそのイオン形式を特定します:
*反応物の化学式を書き留めます。
*電荷を考慮して、各反応物をその構成イオンに分解します。たとえば、NaClはNa⁺イオンとcl⁻イオンに分解します。
2。可能な製品を予測します:
*反応物の陽イオンと陰イオンを交換します。これは、二重変位反応では、陽性イオン(カチオン)がパートナーを切り替えるという考えに基づいています。
3。潜在的な製品の溶解度を決定します:
* 溶解度の表を参照してください: これらのテーブルは、化合物が水に溶けたり、わずかに溶けたり、不溶性であるかを示しています。
* 一般的な溶解度ルール: 一般的な溶解度ルールをガイドラインとして使用することもできます。
* ほとんどのアルカリ金属塩(li⁺、na⁺、k⁺、rb⁺、cs⁺)は可溶性です。
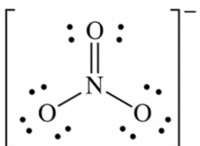
* ほとんどの硝酸塩(no₃⁻)塩は可溶性です。
* ほとんどの塩化物(cl⁻)、臭化物(br⁻)、およびヨウ化物(i⁻)塩は溶けやすい。
* ほとんどの硫酸塩(so₄²⁻)塩は溶けやすいですが、ba²⁺、sr²、ca²⁺、pb²⁺、hg₂²⁺を除きます。
* アルカリ金属とアンモニウム(nh₄⁺)を持つものを除いて、ほとんどの炭酸塩(Co₃²⁻)およびリン酸塩(po₄³⁻)塩は不溶性です。
* ほとんどの水酸化物(OH⁻)塩は不溶性ですが、アルカリ金属とCa²⁺、sr²⁺、ba²⁺を除きます。
4。沈殿物を特定します:
* 不溶性 水には沈殿物があります。解決策から落ち着く固体を形成します。
例:
硝酸銀(Agno₃)と塩化ナトリウム(NaCl)の水溶液を反応しているとしましょう。
1。反応物とイオン:
*agno₃→ag⁺ +no₃⁻
* naCl→na⁺ +cl⁻
2。可能な製品:
*ag⁺ +cl⁻→agcl(塩化銀)
*na⁺ +no₃⁻→nano₃(硝酸ナトリウム)
3。溶解度:
* AgClは水に不溶です(溶解性規則に従って)。
*ナノは水に溶けます。
4。沈殿物:
* agcl 沈殿物です。
したがって、硝酸銀と塩化ナトリウムの反応において、形成された沈殿物は塩化銀(AGCL)です。