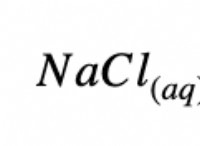* 窒素の不活性性: 窒素は、その原子間の強い三重結合のため、非常に安定した分子です。これにより、比較的非アクティブになります。
* 酸としてのHCl: 塩酸は強酸であり、陽子を容易に寄付することを意味します(H⁺)。しかし、窒素の強力な三重結合を破るのに十分な強力な酸化剤ではありません。
要約: 窒素と塩酸の間の反応性の欠如は、窒素の強力な三重結合と、HClが十分に強力な酸化剤として作用することができないことによるものです。
ただし、いくつかの例外があります:
* 非常に特定の条件下: 窒素は、触媒の存在下や極端に高い温度と圧力でHClと反応する可能性があります。これらの反応は一般に遭遇しません。
* 塩化アンモニウムの形成: 窒素自体は反応しませんが、窒素を含むアンモニア(NH₃)は、HClと反応して塩化アンモニウム(NH₄CL)を形成します。この反応は、単純な酸塩基反応です。
nh₃(g) + hcl(g)→nh₄cl(s)
一般的なルールは、窒素は非常に不活性であり、HClと容易に反応しないことを忘れないでください。