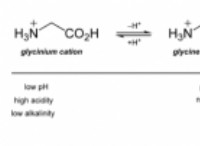
その理由は次のとおりです。
* 水素イオンは非常に反応的です: 彼らは中立になるために電子を獲得する強い傾向を持っています。
* 水分子は極性です: それらは、水素原子に部分的な正電荷と酸素原子に部分的な負電荷を持っています。
* ハイドロニウムイオン形成: 水素イオンの正電荷は、水分子の酸素原子に孤立した電子のペアを引き付け、共有結合を形成します。これにより、ヒドロニウムイオン(H3O+)が生じます。
したがって、溶液中の水素イオンを表すためにH+をしばしば書きますが、水の存在下で水素イオンとして存在することを覚えておくことが重要です。