* 制限反応物: 酸素は制限反応物です このシナリオで。これは、存在する酸素の量が、どのくらいの水素が反応できるかを決定することを意味します。
* 過剰反応物: 水素ガスは過剰反応物です 。酸素が完全に反応するために必要なよりも多くの水素があります。
* 不完全な反応: 反応は、すべての酸素が使い果たされるまで進行します。 いくつかの水素ガスは未反応の上に残されます。
* 製品: 反応は依然として水を生成しますが(H₂O)、形成される水の量は利用可能な酸素の量によって制限されます。
例:
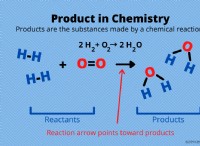
2モルの水素ガス(H₂)と1モルの酸素ガス(O₂)があると想像してください。反応のバランスの取れた化学式は次のとおりです。
2h₂ +o₂→2h₂o
方程式から、2モルの水素が1モルの酸素と反応することがわかります。 この例では、わずか1モルの水素と反応するのに十分な酸素があります。 残りの1モルの水素は残ります。
キーポイント:
*制限反応物は、形成された製品の量を決定します。
*反応が完了した後、過剰な反応物は残されます。
*反応は、制限反応物が完全に消費されるまで進行します。
これ以上質問がある場合はお知らせください!