1。温度を上げる:
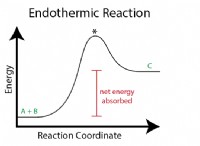
* 原則: ほとんどの固形物の場合、溶解度は温度とともに増加します。 温度を上げると、溶媒分子はより多くのエネルギーを持ち、溶質の結晶格子構造をバラバラにし、より多くの溶質分子を取り入れることができます。
* 例: 砂糖は冷水よりもお湯に溶けます。
2。溶媒を変更します:
* 原則: 異なる溶媒は、同じ溶質に対して異なる溶解度を持っています。 溶質の溶解度が高い溶媒を使用することにより、さらに溶解することができます。
* 例: 塩はエタノールよりも水に溶けます。
3。溶媒を追加:
* 原則: 飽和溶液はすでにその温度に対して最大溶質濃度にありますが、溶媒を追加することで溶液の *体積 *を増やすことができます。 これにより、濃度が希薄になり、より多くの溶質を溶かすことができます。
* 例: 飽和糖溶液があります。より多くの水を追加することにより、溶液が再び飽和になるまで、より多くの砂糖を溶解できます。
4。別の溶質を使用してください:
* 原則: 2つの溶質が互いに反応しない限り、別の溶質(選択した溶媒に溶けやすい場合)を飽和溶液に溶解できます。
* 例: 飽和塩溶液があります。砂糖を塩と同じ溶液に溶かすことができます。
重要な注意: これらの方法は、特定の種類のソリューションと溶質に対してのみ機能します。 これらの変更にさらされたときに、すべてのソリューションが同じように動作するわけではありません。
もっと具体的な例が欲しいかどうか教えてください!