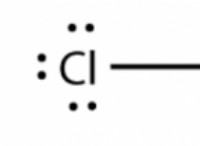反応性:
* それが意味すること: 反応性とは、要素が化学反応にどれほど容易に関与するかを指します。高反応性要素は、反応を迅速かつ簡単に受ける傾向があります。
* なぜそれが起こるのか: 反応性は、元素の原子、特に最も外側のシェル(価電子)の電子の電子の配置によって決定されます。 ほぼ完全または空の外側のシェルを備えた要素は、安定した構成を実現するために反応する可能性が高くなります(貴重なガスのような)。
イオン形成:
* それが意味すること: イオンは、電子を獲得または失った原子であり、正味の正または負の電荷を与えます。
* なぜそれが起こるのか: イオンを形成する要素は、電子構成が電子を獲得または失うためにエネルギー的に好まれるため、簡単にそうすることができます。
それをまとめる:
元素が反応性であり、イオンを簡単に形成すると言うとき、それは次のことを意味します。
* それらの原子は他の原子と容易に相互作用して結合を形成し、化学反応につながります。
* 彼らは安定した電子構成を達成するために電子を獲得または失う傾向があり、イオンの形成をもたらします。
例:
* ナトリウム(Na)は非常に反応性のある要素です。 1つの価電子があります。この電子を容易に失い、積極的に帯電したナトリウムイオン(Na+)になり、Noble Gas Neonと同様の安定した電子構成を達成します。
* 塩素(Cl)も反応性があります。 7つの価電子を持ち、1つの電子を容易に獲得して負に帯電した塩化物イオン(Cl-)になり、Noble Gas Argonと同様の安定した電子構成を実現します。
要するに、イオンを簡単に形成する反応性の要素は、原子が電子を再配置して安定した状態を達成することに熱心な要素であり、多くの場合、電子を失い、摂取してイオンになります。