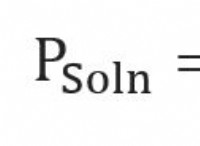* 電子親和性: 塩素は、臭素よりも電子親和性が高い。これは、塩素が電子に対してより強い魅力を持っていることを意味し、電子を獲得して負のイオンを形成する可能性が高くなります。
* 原子サイズ: 塩素は臭素よりも小さい。このサイズは、塩素の最も外側の電子が核によってよりしっかりと保持され、電子のより強い引力をもたらすことを意味します。
* 電気陰性度: 塩素は、臭素よりも電気陰性度が高い。電気陰性度は、結合中に電子を引き付ける原子の能力の尺度です。より高い電気陰性度は、塩素が電子をそれ自体に引き寄せる可能性が高いことを意味し、より反応的になります。
簡単に言えば: 塩素は、電子をつかんで外殻を完成させることに熱心であり、そのサイズが小さくなると、それが容易になります。
反応性のこの違いは、塩素が臭素よりも強い酸化剤である理由です。