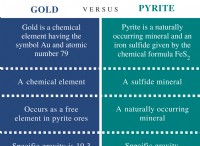
* 他のイオンの電荷を特定します:
*マグネシウム(mg)は周期表のグループ2にあるため、+2電荷(mg²⁺)があります。
*硫酸塩(SO₄)は、-2電荷(SO₄²⁻)を持つ多原子イオンです。
* 料金のバランス: 電荷は等しく反対であるため、それらは互いにキャンセルされ、ニュートラル化合物(mgso₄)が生じます。
* 硫黄の原子価:を決定します 硫酸イオンでは、硫黄は4つの酸素原子(O)に結合します。各酸素原子の電荷は-2で、合計負電荷は-8です。これのバランスをとるには、硫黄に+6の充電が必要です。
したがって、Mgso₄の硫黄の原子価は+6です。