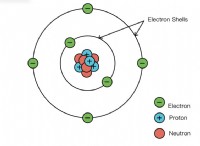
* 電子構成: ナトリウム(NA)には11個の電子があります。その電子構成は2、8、1です。これは、最も外側のシェル(価数シェル)に1つの電子があることを意味します。
* 安定性: 原子は、安定性のために電子の完全な外殻を持つように努力しています。ナトリウムは、単一の原子価電子を失うことでこれを達成できます。
* イオン形成: ナトリウムが電子を失うと、11陽子(正電荷)と10電子(負電荷)のみがあるため、正の帯電イオン(陽イオン)になります。
* チャージ: 陽子と電子の数の違いは、イオンの電荷を決定します。 ナトリウムは1つの電子を失うため、その電荷は+1です。
要約: ナトリウムは1つの電子を失い、より安定になり、+1電荷が発生します。